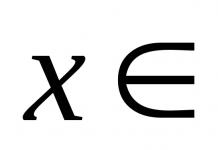Краткое описание:
Сазонов В.Ф. Ионные каналы мембраны [Электронный ресурс] // Кинезиолог, 2009-2017: [сайт]. Дата обновления: 31.01.2017..__.201_). _Обзор ионных каналов мембраны. Определение понятия "ионные каналы", их строение, свойства, функции, функциональные состояния, функциональная классификация.
Введение
Ионные каналы (ИК) клеточной мембраны имеют огромное значение для жизни клеток. Они обеспечивают обмен клетки с окружающей средой веществом, энергией и информацией, с них начинаются и ими поддерживаются процессы возбуждения и торможения в нервной системе и мышцах, именно они (вместе и другими молекулярными рецепторами) обеспечивают восприятие клеткой внешних сигналов. С помощью ИК происходит передача в клетку управляющих сигналов из окружающей её среды. Именно ИК обеспечивают синаптическую передачу возбуждения от возбуждённого нейрона на другие клетки. Обобщая, можно сказать, что почти все важнейшие физиологические процессы в организме начинаются с ионных каналов и поддерживаются ими!
Определение понятия
Ионные каналы мембраны - это маленькие белковые трубочки разного диаметра, вставленные в клеточную мембрану, через которые внутрь клетки или наружу могут перемещаться ионы. Перемещение ионов через ионные каналы приводит к изменению концентрации ионов внутри и снаружи клетки, а также к изменению электрического потенциала мембраны. Перемещение в клетку ионов кальция через кальциевые каналы запускает в ней различные внутренние биохимические процессы. Существует множество видов ионных каналов. © 2014-2017 Сазонов В.Ф. © 2014-2016 kineziolog.bodhy.ru..
Ионный канал клеточной мембраны - это отверстие в мембране, обмётанное по краям белковой нитью, через которое через мембрану могут перемещаться ионы. Белковая нить нужна для того, чтобы отверстие не затянулось жировым слоем мембраны. Во многих случаях белковая нить, или каналообразующий белок, обладает функциональной активностью и контролирует пропускную способность канала по отношению к различным ионам. © 2014-2017 Сазонов В.Ф. © 2014-2016 kineziolog.bodhy.ru..
Итак, ионные каналы (ИК) - это сложные трансмембранные белковые структуры, пронизывающие клеточную мембрану поперёк в виде нескольких петель и образующие в мембране сквозное отверстие (пору). Канальные белки состоят из субъединиц, образующих структуру со сложной пространственной конфигурацией, в которой кроме поры обычно имеются дополнительные молекулярные системы: открытия, закрытия, избирательности, инактивации, рецепции и регуляции. ИК могут иметь не один, а несколько участков (сайтов) для связывания с управляющими веществами (лигандами).
Ионные каналы можно рассматривать как транспортный механизм , обеспечивающий перемещение ионов между цитоплазмной клетки и наружной средой.
Кроме ИК в мембране суцществуют и другие транспортные системы для переноса через неё различных веществ (смотрите транспортные механизмы мембраны). Так, перенос веществ может осуществляться специальными транспортными белками , или транслоказами . Транслоказы - это несколько иное понятие, чем ИК. В отличие от мембранных каналов , транслоказы в процессе переноса вещества через мембрану взаимодействуют с ним как с лигандом и при этом претерпевают конформационные изменения . По кинетике перенос веществ с помощью транслоказ в виде облегчённой диффузии напоминает ферментативную реакцию.
Упрощённое определение:
Ионные каналы - это поры (дырочки) в клеточной липидной мембране, которые "обшиты" по краям белковой нитью, чтобы дырочки не затянулись. Эти поры могут становиться пошире или поуже: либо сами по себе, либо при определённых воздействиях. Каналы могут иметь разное строение, поэтому разные виды каналов имеют разную проницаемость, избирательность и управляемость.
Итак, ионный канал - это интегральный белок, образующий в мембране пору для обмена клетки с окружающей средой ионами K + , Na + , H + , Ca 2+ , Cl - , а также водой, и способный изменять свою проницаемость.
Аквапорины - водные неионные каналы мембраны
В мембране существуют и неионные каналы. Например, аквапорины - это специальные водные каналы , пропускающие через себя воду. Это тоже мембранные каналы, хотя их формально нельзя назвать "ионными каналами".
Пространственная структура канального белка-аквапорина представляет собой цилиндрический канал, по которому движутся молекулы воды. Через него проходит вода и только вода, но не ионы. Аминокислоты в этом белке расположены таким образом, что полярность создаваемого ими электростатического поля переключается в центре канала на обратную. Поэтому молекулы воды, дойдя до середины канала, переворачиваются так, что их дипольные моменты в верхней и нижней части канала оказываются направленными в противоположные стороны. Такое переориентирование предотвращает просачивание через канал заряженных ионов. Аквапорин не пропускает даже ионы гидроксония H3O+ (то есть гидратированные протоны, или ионы водорода), от концентрации которых зависит кислотность среды. При этом клеточный мембранный "водопровод" обладает потрясающей пропускной способностью: он пропускает до миллиарда молекул воды в секунду. Сейчас известно уже около 200 разновидностей белков водных каналов у растений и животных, в том числе 11 - у человека. Благодаря аквапоринам клетки не только регулируют свой объём и внутреннее давление, но и выполняют такие важные функции, как всасывание воды в почках животных и корешках растений.
В настоящее время в молекулярной биологии в основном завершён описательный период в исследовании многообразия катион-транспортирующих ионных каналов в клетках эукариот. Теперь на первый план выходят проблемы познания механизмов регуляции ионных каналов и описание их участия в реакциях живой клетки на различные воздействия и на изменение её микроокружения.
Регулирумый перенос ионов через гидрофильные поры мембраны с помощью управляемых ИК является важнейшим свойством живых клеток, как электровозбудимых, так и невозбудимых.
В связи с этим целесообразно использовать в классификации ионных каналов именно принцип управления их деятельностью. Принцип управления состоянием ионных каналов и был положен в основу предложенной нами () функциональной классификации ионных каналов.
Видео: Ионные каналы в мембране
Строение ИК
ИК состоят из белков сложной структуры (белков-каналоформеров). Схематические изображения ИК приведены ниже, например: .
На рисунке справа показан натриевый канал: вид сверху, с наружной стороны мембраны (Источник: Horn R. (2011). Peering into the spark of life . Nature 475 , 305–306).
Белки ИК имеют определённую конформацию, образующую трансмембранную пору, и "вшиты" в липидный слой мембраны. Канальный белковый комплекс может состоять либо из одной белковой молекулы, либо из нескольких белковых субъединиц, одинаковых или разных по строению. Эти субъединицы могут кодироваться разными генами, синтезироваться на рибосомах по-отдельности и затем собираться в виде целостного канала. В другом случае канал может представлять собой единый полипептид, который в виде петель прошивает мембрану несколько раз. На начало XXI века известно более 400 белков-каналоформеров, для биосинтеза которых используется 1-2% генома человека.
Домены - это отдельные компактно оформленные части канального белка или субъединиц. Сегменты - это части белкка-каналоформера, свёрнутые спирально и прошивающие мембрану. Концевые домены белка-каналоформера (N- и С-терминальные домены) могут торчать из мембраны как наружу, так и внутрь клетки.
Практически все ИК имеют в составе своих субъединиц регуляторные домены , способные связываться с различными управляющими веществами (регуляторными молекулами) и за счёт этого менять состояние или свойства канала. В потенциал-активируемых ИК один из трансмембранных сегментов содержит специальный набор аминокислот с положительными зарядами и работает как сенсор электрического потенциала мембраны. При изменении потенциала такой сенсор меняет состояние канала с открытого на закрытое или наоборот. Таким образом, ИК могут управляться определёнными воздействиями извне, это важное их свойство.
ИК в своём составе могут иметь также вспомогательные субъединицы , выполняющие модуляторные, структурные или стабилизирующие функции. Один класс таких субъединиц - внутриклеточные, расположенные полностью в цитоплазме, а второй - мембранные, т.к. они имеют трансмембранные домены, прошивающие мембрану.
По структуре ИК возможно провести их классификацию, о чём будет сказано ниже.
Свойства ИК
Селективность - это избирательная повышенная проницаемость ИК для определённых ионов. Для других ионов проницаемость понижена. Такая избирательность определяется селективным фильтром - самым узким местом канальной поры. Фильтр, кроме узких размеров, может иметь также локальный электрический заряд. Например, катион-селективные каналы обычно имеют в области своего селективного фильтра отрицательно заряженные остатки аминокислот в составе белковой молекулы, которые притягивают положительные катионы и отталкивают отрицательные анионы, не пропуская их через пору.
Управляемая проницаемость - это способность ИК открываться или закрываться при определённых управляющих воздействиях на канал. Понятно, что закрытый канал имеет пониженную проницаемость, а открытый - повышенную. По этому свойству ИК можно классифицировать в зависимости от способов их открытия: например, потенциал-активируемые, лиганд-активируемые и т.д.
Инактивация - это способность ИК через некоторое время после своего открытия автоматически понижать свою проницаемость даже в том случае, когда открывший их активирующий фактор продолжает действовать.
Быстрая инактивация - это особый процесс со своим особым механизмом, отличающийся от медленного закрытия канала (медленной инактивации). Закрытие (медленная инактивация) канала происходит за счёт процессов, противоположных процессам, обеспечившим его открытие, т.е. за счёт изменения конформации канального белка. А вот, например, у потенциал-активируемых каналов быстрая инактивация происходит с помощью специальной молекулярной "пробки-затычки", напоминающей пробку на цепочке, которую обычно используют в ваннах. Эта пробка представляет собой аминокислотную (полипептидную) петлю с утолщением на конце в виде трёх аминокислот, которым и затыкается внутреннее устье канала со стороны цитоплазмы. Именно поэтому потенциал-зависимые ИК для натрия, обеспечивающие развитие потенциала действия и движение нервного импульса, могут пропускать в клетку ионы натрия только в течение нескольких миллисекунд, а затем они автоматически закрываются своими молекулярными пробками, несмотря на то, что открывающая их деполяризация продолжает действовать. Другим механизмом инактивации ИК может служить модификация дополнительными субъединицами внутриклеточного устья канала.
Блокировка - это способность ИК под действием веществ-блокаторов фиксировать какое-то одно своё состояние и не реагировать на обычные управляющие воздействия. В таком состоянии канал просто перестаёт давать ответы на управляющие воздействия. Блокировку вызывают вещества-блокаторы , которые могут называться антагонистами , блокаторами или литиками .
Антагонисты - это вещества, препятствующие активирующему действию других веществ на ИК. Такие вещества способны хорошо связываться с рецепторным участком ИК, но не способны изменить состояние канала, вызвать его ответную реакцию. Получается блокада рецептора и вместе с ним - блокада ИК. Следует помнить, что антагонисты не обязательно вызывают полную блокаду рецептора и его ИК, они могут действовать более слабо и лишь ингибировать (угнетать) работу канала, но не прекращать её полностью
Агонисты-антагонисты - это вещества, которые обладают слабым стимулирующим влиянием на рецептор, но при этом блокируют действие естественных эндогенных управляющих веществ.
2. Потенциал-управляемые (потенциал-чувствительные, потенциал-зависимые, потенциал-активируемые, voltage-gated). Так, потенциал-управляемые натриевые каналы открываются под действием сдвига электрического потенциала мембраны, превышающего критический уровень деполяризации. Поэтому при достижении определённого порогового уровня деполяризации мембраны они открываются, а при обратном снижении уровня деполяризации - оказываются закрытыми. Но важно знать то, что ещё до обратного снижения уровня деполяризации эти каналы закрываются с внутренней стороны специальными белковыми "пробками" и это происходит автоматически, незасисимо от изменений деполяризации. Вследствие этого потенциал-управляемые натриевые ИК находятся в открытом состоянии всего несколько миллисекунд, а потом закрываются "пробкой", т.е. инактивируются. Окончательно они переходят в закрытое состояние при реполяризации и восстановлении потенциала покоя. Как при химической, так и при фармакологической модификации таких ИК у них сохраняется основной механизм активации и инактивации в ответ на сдвиг мембранного потенциала, что и определяет быстрые изменения катионной проницаемости возбудимых мембран за счёт потенциал-управляемых ИК. Именно такого типа потенциал-управляемые натриевые ИК обеспечивают перемещение нервного импульса по мембране нейрона (смотри: потенциал действия и нервный импульс). Такие потенциал-зависимые натриевые каналы I открываются на уровне КУД, т.е. -55mV, они и формируют потенциал действия и нервный импульс.
Примеры: тетродотоксин-чувствительные натриевые каналы, потенциал-активируемые К-каналы, калиевые Kdr-каналы задержанного выпрямления, кальциевые каналы пресинаптических окончаний аксонов .
На рисунке справа - условная схема работы потенциал-управляемого ИК (кликните на рисунок, чтобы увидеть процесс в динамике).
3. Хемо -управляемые (хемочувствительные, хемозависимые, лиганд-управляемые, лиганд-зависимые, рецептор-активируемые). Они открываются при связывании с рецепторным участком канала специфического лиганда (управляющего вещества: трансмиттера или его миметика). Такие каналы обычно локализованы в химических синапсах на их постсинаптических мембранах и преобразуют химический сигнал, возникающий за счёт пресинаптического высвобождения нейромедиатора, в постсинаптический электрический локальный потенциал. Смотри: локальный потенциал , 3_3 Синапсы , синапсы, медиаторы и модуляторы .
Примеры: каналы с никотиновыми ацетилхолиновыми рецепторами nAChR), серотониновыми рецепторами (5-HT3), глициновыми, ГАМК-рецепторами (GABAA и GABAC).
На рисунке справа - лиганд-управляемый ионный канал с никотиновым ацетилхолиновым рецептором (никотин - миметик, ацетилхолин - трансмиттер). Канал состоит из 5 субъединиц и поры в центре. Вверху - поперечный разрез этих субъединиц: a1, a2, b, g, d. Внизу - участки субъединиц, образующих «воротную систему» канала. Представлены аминокислотные последовательности М2 a-спирали в b- и d-. Из 5 субъединиц, образующих пору, изображены лишь 4, а ближайшая к нам удалена, чтобы были видны участки М2, облицовывающие ионный канал, и ворота. Видно, что большая часть молекулы белка выходит за пределы внешней поверхности плазматической мембраны, образуя молекулярные рецепторы к лиганду. Каждая из двух a-субъединица содержит связывающий центр для ацетилхолина, следовательно, с рецептором может связаться 2 молекулы лиганда (нейротрансмиттера или нейромиметика). Ворота, находящиеся в пределах поры, открываются при связывании ацетилхолина с рецепторным участком канала. Отрицательно заряженные остатки глутаминовой и аспарагиновой аминокислот (они выделены синим цветом) имеются в обоих концах М2-спиралей, т.е. с двух сторон поры, благодаря чему предотвращается вход в канал анионов, а катионы Na + и К + при его закрытом состоянии могут быть связаны уже в самом канале.
Видео: Работа хемо-управляемого (лиганд-управляемого) ионного канала
4. Стимул-управляемые (механочувствительные, механосенситивные, стретч-активируемые, stretch-activated, протон-активируемые, температурно-чувствительные).
Они открываются под воздействием специфичного и адекватного для них стимула (раздражителя). Такие каналы обеспечивают сенсорное восприятие и располагаются в мембране сенсорных рецепторов.
Пример: механочувствительные ИК
рецепторных волосковых клеток, обеспечивающих слуховое восприятие; температурно-чувствительные ИК
терморецепторов кожи, обеспечивающие восприятие тепла и холода.
В настоящее время стимул-управляемые механочувствительные ИК обнаружены не только в специализированных механорецепторных структурах, но также и в мембранах бактерий, грибов, растений, позвоночных и беспозвоночных животных. Механочувствительные каналы не только обеспечивают сенсорное восприятие механического раздражения, но также вовлечены в контроль клеточного цикла, регуляцию объёма и роста клеток, секрецию и эндоцитоз.
TRP-каналы в мембране терморецепторов кожи обеспечивают термотрансдукцию, открываясь при различных значениях темпераруры. Они пропускают катионы, особенно ионы кальция.
5. Совместно-управляемые (NMDA-рецепторно-канальный комплекс). Они открываются одновременно как лигандами, так и определённым электрическим потенциалом мембраны. Можно сказать, что у них двойное управление.
Пример: NMDA-рецепторно-канальный комплекс , имеющий сложную систему управления, включающую в себя 8 рецепторных участков-сайтов, с которыми могут связываться различные лиганды.
6. Опосредованно -управляемые (вторично-управляемые, ион-активируемые, ион-зависимые, мессенджер-управляемые, управляемые метаботропными рецепторами). Они открываются и закрываются не под действием прямых внешних сигналов, а вследствие опосредованного воздействия на них внутриклеточных вторичных мессенджеров (ионов кальция Са 2+ , цАМФ, цГМФ, ИФ3, диацилглицерола). Основной механизм такого управления - фосфорилирование ионного канала с внутренней стороны мембраны.
Опосредованное вторичными мессенджерами управление является не прямым, а вторичным. Оно зависит не только от внешнего воздействующего сигнала, но и от наличия, концентрации и активности вторичных мессенджеров. Пусковым сигналом к началу этого процесса может служить воздействие на так называемый метаботропный рецептор , не относящийся к структуре самого управляемого ионного канала и расположенный на мембране где-то отдельно от него. Воздействие на метаботропный рецептор приводит к повышению в клетке концентрации вторичных посредников-мессенджеров. Это ионы Са 2+ , цАМФ, цГМФ, ИФ3, диацилглицерол. Они активируют соответствующие ферменты-протеинкиназы: А-киназы (цАМФ-зависимые), G-киназы (цГМФ-зависимые), В-киназы (кальций-кальмодулин-зависимые) или С-киназы (кальций-фосфолипид-зависимые). В свою очередь, активированные киназы фосфорилируют ИК мембраны изнутри клетки, т.е. присоединяют к ним фосфаты. В результате этого канал может перейди надолго в новое состояние (открытое или, наоборот, закрытое). После срезания фосфатов ферментом фосфатазой канал возвращается к своему прежнему состоянию. В некоторых случаях такой вторичный мессенджер, как G-белок в виде своей активной субъединицы бета-гамма может сам присоединиться к ионному каналу и поменять его состояние. Так, например, могут открываться (активироваться) калиевые каналы при раздражении ацетилхолином мускариновых рецепторов, связанных с G-белком.
Примеры: Са 2+ -активируемые хлорные каналы, кальций-активируемые калиевые каналы, цГМФ-активируемые натриевые каналы палочек сетчатки глаза .
Вот, например, опосредованные ион-управляемые кальций-активируемые хлорные каналы являются одним из основных компонентов системы эпителиальной секреции, сенсорной трансдукции , регулирования нейронной и сердечной возбудимости у животных. В клетках растений кальций-активируемые хлорные каналы ответственны за состояние тургора клетки. При повышении концентрации ионов кальция внутри клетки эти каналы открываются и начинают пропускать ионы хлора.
К опосредованно-управляемым (мессенджер-управляемым) ионным каналам формально можно отнести также все каналы, которые управляются "изнутри" с помощью посредников - вторичных мессенджеров. Такой способ управления чаще всего является дополнительным по отношению к "внешнему управлению", и получается, что к мессенджер-управляемым каналам относится большинство каналов из других групп нашей функциональной классификации. Например, все те ИК, которые могут подвергаться фосфорилированию.
7. Актин-управляемые (актин-регулируемые, actin-regulated, actin-gated channels). Они открываются и закрываются за счёт разборки-сборки примембранных микрофиламентов с участием актин-связывающих белков.
В электроневозбудимых клетках активация и инактивация актин-управляемых потенциал-независимых натриевых каналов контролируется процессами разборки-сборки примембранных микрофиламентов с участием актин-связывающих белков. Актиновые элементы цитоскелета, по-видимому, представляют важнейшую часть потенциал-независимого воротного механизма, управляющего открыванием и закрыванием каналов. Именно сборка микрофиламентов на цитоплазматической стороне мембраны приводит к инактивации таких каналов.
8. Коннексоны (двойные поры). Образуют в мембранах контактирующих клеток сквозные непрерывные каналы через две мембраны сразу в зоне щелевых контактов для взаимного обмена веществами между этими клетками. Через коннексоны передаются электрические сигналы, аминокислоты и небольшие молекулы управляющих веществ: цАМФ, InsP 3 , аденозин, АДФ и АТФ. Они состоят из 6 белковых субъединиц (коннексинов), живущих всего несколько часов. Коннексины - это политопные интегральные мембранные белки 4 раза прошивающие мембрану, имеющие две внеклеточные петли (EL-1 и EL-2), цитоплазматическую петлю (CL) с N-концом (AT) и C-концом (CT), вдающимися в цитоплазму. Через коннексоны соединяется внутренняя среда соседствующих клеток.
Коннексоны являются "неспецифически-управляемыми" каналами. Их состояние регулируется pH, электрическим потенциалом, ионами Са 2+ , фосфорилированием и другими факторами.
Коннексоны найдены практически во всех видах клеток.
9. «Энерго-зависимые транспортёры» (ионные насосы, ионные помпы, ионные обменники, транспортёры). Это особая группа динамичных пор, проводящих ионы через мембрану, которые формально не относятся к ИК. Их деятельность обеспечивается энергией расщепления АТФ. Они представлены мембранными ферментными белками АТФазами, которые активно протаскивают через себя ионы, используя для этого энергию расщепления АТФ, и обеспечивают активный транспорт ионов через мембрану даже против их градиента концентрации.
Примеры: натрий-калиевый насос, протонный насос, кальциевый насос .
Примеры ионных каналов разного типа

Ацетилхолиновый рецептор лиганд-управляемого (хемозависимого) ионного канала
На рисунке слева представлена структурная модель лиганд-управляемого ацетилхолинового ИК.
селективные (проницаемы только для одного вида ионов). По характеру ионов, которые они пропускают на Na+, Ca++, Cl-, K+-каналы;
неселективные (проницаемы для нескольких видов ионов);
2) По способу регуляции делятся на:
потенциалзависимые (электровозбудимые, потенциалуправляемые)
Потенциалнезависимые (хемовозбудимые, (лиганд-рецептор -зависимые), хемоуправляемые)
Механовозбудимые (механоуправляемые).
Потенциал покоя и действия. Мембранно-ионная теория происхождения потенциала покоя и действия. Местное и распространяющееся возбуждение.

Установлено, что
мембрана любой живой клетки поляризована,
внутренняя поверхность элетроотрицательна
по отношению к наружной. Мембранный
потенциал равен - (минус) 70 - (90) мв. При
возбуждении происходит снижение величины
исходного потенциала покоя с перезарядкой
мембраны. Формирование и сохранение
потенциала покоя обусловлено непрерывным
движением ионов по ионным каналам
мембраны, постоянно существующей
разностью концентраций катионов по обе
стороны мембраны, непрерывной работой
натрий-калиевого насоса. За счет
постоянного удаления из клетки иона
натрия и активного переноса в клетку
иона калия сохраняется разность
концентраций ионов и поляризация
мембраны. Концентрация иона калия в
клетке превышает внеклеточную концентрацию
в 30 - 40 раз, внеклеточная концентрация
натрия примерно на порядок выше
внутриклеточной. Электроотрицательность
внутренней поверхности мембраны
обусловлена наличием в клетке избытка
анионов органических соединений,
абсолютная величина потенциала покоя
(мембранный потенциал, трансмембранный
потенциал, равновесный калиевый
потенциал) обусловлена главным образом
соотношением внутри- и внеклеточной
концентраций ионов калия и удовлетворительно
описывается уравнением Нернста
:
 (1)
(1)
Современная теория учитывает так же:
1) разницу концентраций ионов натрия, хлора, кальция;
2) проницаемость (Р) мембраны для каждого иона в текущий момент времени.
Наличие потенциала покоя позволяет клетке практически мгновенно после действия раздражителя перейти из состояния функционального покоя в состояние возбуждения.
Возникновение потенциала действия (деполяризация)

I – мембранный потенциал
1 - потенциал покоя, 2-- медленная деполяризация, 3 - быстрая деполяризация, 4 - быстрая реполяризация, 5 – медленная реполяризация, 6- гиперполяризация
II - возбудимость
а – нормальная, б – повышенная, в –абсолютная рефрактерность,
г – относительная рефрактерность, д – супернормальность,
е -субнормальность
Потенциал действия (ПД) развивается при наличии исходной поляризации мембраны (потенциала покоя) благодаря изменению проницаемости ионных каналов (натриевых и калиевых). После действия раздражителя потенциал покоя уменьшается, активация каналов повышает их проницаемость для ионов натрия , который входит в клетку и обеспечивает процесс деполяризации. Поступление в клетку иона натрия уменьшает электроотрицательность внутренней поверхности мембраны, что способствует активации новых ионных натриевых каналов и дальнейшему поступлению в клетку иона натрия. Действуют силы:
а) электростатическое притяжение внутриклеточных анионных группировок;
б) концентрационный градиент ионов натрия, направленный внутрь клетки.
Пик потенциала действия обусловлен равновесием поступления в клетку ионов натрия и равным их удалением под влиянием сил отталкивания одноимённо заряженных ионов.
Для различных веществ и, в частности, для минеральных ионов имеет исключительно важное значение в жизнедеятельности клетки и особенно в механизмах восприятия, преобразования, передачи сигналов от клетки к клетке и на внутриклеточные структуры.
Определяющую роль в состоянии проницаемости мембран клетки имеют их ионные каналы, которые формируются каналообразующими белками . Открытие и закрытие этих каналов могут контролироваться величиной разности потенциалов между наружной и внутренней поверхностями мембраны, множеством сигнальных молекул (гормонов, нейромедиаторов, сосудоактивных веществ) вторичными посредниками передачи внутриклеточных сигналов, минеральными ионами.
Ионный канал — несколько субъединиц (интегральных мембранных белков, содержащих трансмембранные сегменты, каждый из которых имеет а-спиральную конфигурацию), обеспечивающих перенос ионов через мембрану.
Рис. 1. Классификация ионных каналов
Современные представления о строении и функции ионных каналов стали возможными благодаря разработке методов регистрации электрических токов, протекающих через изолированный участок мембраны, содержащий одиночные ионные каналы, а также благодаря выделению и клонированию отдельных генов, контролирующих синтез белковых макромолекул, способных формировать ионные каналы. Это позволило искусственно модифицировать структуру таких молекул, встраивать их в мембраны клеток и изучать роль отдельных пептидных участков для выполнения функций каналов. Оказалось, что каналообразующие белковые молекулы всех ионных каналов имеют некоторые общие признаки строения и обычно представлены большими трансмембранными белками с молекулярными массами выше 250 кД .
Они состоят из нескольких субъединиц. Обычно важнейшие свойства каналов определяются их а-субъединнней . Эта субъединица принимает участие в формировании ионоселективной норы, сенсорного механизма трансмембранной разности потенциалов — ворот канала и имеет места связывания для экзогенных и эндогенных лигандов. Другие субъединицы, входящие в структуру ионных каналов, играют вспомогательную роль, модулирующую свойства каналов (рис. 2).
Каналообразующая белковая молекула представлена внемембранными аминокислотными петлями и внутримембранными спирализованными участками-доменами, образующими субъединицы ионных каналов. Белковая молекула сворачивается в плоскости мембраны так, что между контактирующими друг с другом доменами и формируется собственно ионный канал (см. рис. 2, внизу справа).
Каналообразующая молекула белка располагается в цитоплазматической мембране так, что ее трехмерная пространственная структура формирует устья канала, обращенные к наружной и внутренней сторонам мемораны, пору, заполненную водой, и «ворота». Последние образуются участком пептидной цепи, который может легко изменять свою конформацию и определять открытое или закрытое состояние канала. От размеров поры и ее заряда зависят селективность и проницаемость ионного канала. Проницаемость канала для данного иона определяется также его размерами, величиной заряда и гидратной оболочкой.

Рис. 2. Строение Na+ -ионного канала клеточной мембраны: а — двухмерное строение а-еубъединицы ионного канала клеточной.мембраны; б — слева — натриевый канал, состоящий из а-субъединнцы и двух Р-субъединнн (вид сбоку); справа — вил натриевого канала сверху. Цифрами I. II. III. IV отмечены домены а-субъединицы
Типы ионных каналов
Описано более 100 разновидностей ионных каналов, для классификации которых используют различные подходы. Один из них основан на учете различий в строении каналов и в механизмах функционирования. При этом ионные каналы можно разделить на несколько типов:
- пассивные ионные каналы, или каналы покоя;
- каналы щелевых контактов;
- каналы, состояние которых (открытое или закрытое) контролируется влиянием на их воротный механизм механических факторов (механочувствительные каналы), разности потенциалов на мембране (потенциалзависимые каналы) или лигандов, связывающихся с каналообразующим белком на внешней или внутренней стороне мембраны (лигандзависимые каналы).
Пассивные каналы
Отличительной особенностью этих каналов является то, что они могут быть открытыми (активными) в покоящихся клетках, т.е. в отсутствие каких-либо воздействий. Это предопределяет их второе название — пассивные каналы. Они не являются строго селективными, и через них мембрана клетки может «протекать» для нескольких ионов, например К+ и CI+ К+ и Na+. Поэтому иногда эти каналы называют каналами утечки. Благодаря перечисленным свойствам каналы покоя играют важную роль в возникновении и поддержании на цитоплазматической мембране клетки мембранного потенциала покоя, механизмы и значение которого обсуждаются далее. Пассивные каналы представлены в цитоплазматических мембранах нервных волокон и их окончаний, клеток поперечно-полосатой, гладкой мускулатуры, миокарда и других тканей.
Механочувствительные каналы
Состояние проницаемости этих каналов изменяется при механических воздействиях на мембрану, вызывающих нарушение структурной упаковки молекул в мембране и ее растяжение. Эти каналы широко представлены в механорецепторов сосудов, внутренних органов, кожи, поперечно-полосатых мышц, гладких миоцитов.
Потенциалзависимые каналы
Состояние этих каналов управляется силами электрического поля, создаваемого величиной разности потенциалов на мембране. Потенциалзависимые каналы могут находиться в неактивном (закрытом), активном (открытом) и инактивированном состояниях, которые контролируются положением активационных и инактивационных ворот, зависящим от разности потенциалов на мембране.
В покоящейся клетке потенциалзависимый канал находится обычно в закрытом состоянии, из которого он может быть открыт или активирован. Вероятность его самостоятельного открытия невысокая, и в состоянии покоя лишь небольшое количество этих каналов в мембране открыто. Уменьшение трансмембранной разности потенциалов (деполяризация мембраны) вызывает активацию канала, повышая вероятность его открытия. Предполагается, что функцию активационных ворот выполняет электрически заряженная аминокислотная группа, закрывающая вход в устье канала. Эти аминокислоты являются сенсором разности потенциалов на мембране; при достижении определенного (критического) уровня деполяризации мембраны заряженная часть молекулы сенсора смещается в сторону липидного микроокружения каналообразующей молекулы и ворота открывают вход в устье канала (рис. 3).
Канал становится открытым (активным) для перемещения через него ионов. Скорость открытия активационных ворот может быть низкой и очень высокой. По этому показателю потенциалзависимые ионные каналы делят на быстрые (например, быстрые потенциалзависимые натриевые каналы) и медленные (например, медленные потенциалзависимые кальциевые каналы). Быстрые каналы открываются мгновенно (мкс) и остаются открытыми в среднем в течение 1 мс. Их активация сопровождается быстрым лавинообразным возрастанием проницаемости канала для определенных ионов.
Способностью изменять свою конформацию обладает другая часть пептидной цепи, представляющая собой аминокислотную последовательность в виде плотного шарика (клубка) на нити, располагающегося у выхода другого устья канала. При изменении знака заряда на мембране шарик закрывает выход из устья, канал становится непроницаемым (инактивированным) для иона. Инактивация потенциалзависимых ионных каналов может осуществляться с помощью других механизмов. Инактивация сопровождается прекращением перемещения ионов через канал и может протекать так же быстро, как активация, или медленно — в течение секунд и даже минут.

Рис. 3. Воротным механизм потенциалозависимых натриевых (вверху) и калиевых (внизу) каналов
Для восстановления исходных свойств ионных каналов после их инактивации необходимо возвратить исходные пространственную конформацию каналообразующего белка и положение ворот. Это достигается при восстановлении разности потенциалов мембраны (реполяризации) до уровня, характерного для состояния покоя клетки или спустя некоторое время после инактивации при сильном воздействии на мембрану. Переход из состояния инактивации в исходное (закрытое) состояние получил название реактивации канала. Будучи реактивированным, ионный канал вновь возвращается в состояние готовности к его повторному открытию. Реактивация потенциалзависимых каналов мембраны также может быть быстрой и медленной.
Потенциалзависимые ионные каналы обычно являются высокоселективными и играют решающую роль в возникновении возбуждения (генерации потенциалов действия), передаче информации по нервным волокнам в виде электрических сигналов, инициировании и регуляции сокращения мышц. Эти каналы широко представлены в мембранах афферентных, эфферентных нервных волокон, в мембранах поперечно-полосатых и гладких миоцитов.
Потенциапзависимые ионные каналы встроены в мембрану нервных окончаний чувствительных нервов (дендритов), иннервирующих пульпу зуба, слизистую оболочку полости рта, где их открытие обеспечивает преобразование рецепторного потенциала в нервный импульс и его последующее проведение по афферентному нервному волокну. С помощью этих импульсов в ЦНС передается информация о всех видах сенсорных ощущений, возникших у человека в полости рта (вкус, температура, механические давления, боль). Подобные каналы обеспечивают возникновение нервных импульсов на мембране аксонного холмика нейронов и его проведение по эфферентным нервным волокнам, преобразование постсинаптических потенциалов в потенциалы действия постсинаптических эффекторных клеток. Примером таких процессов может быть генерация нервных импульсов в моторных нейронах ядра тройничного нерва, которые затем передаются по его эфферентным волокнам к жевательным мышцам и обеспечивают инициирование и регуляцию жевательных движений нижней челюсти.
При исследовании тонких механизмов функционирования потенциалзависимых ионных каналов было выявлено, что существуют вещества, способные блокировать работу этих каналов. Одним из первых среди них было описано вещество тетродотоксин — сильнейший яд, образующийся в организме рыбы фугу. Под его действием наблюдалась блокада потенциалзависимых натриевых каналов в эксперименте, а при его введении в организм животных отмечались потеря чувствительности, расслабление мышц, обездвиженность, остановка дыхания и смерть. Такие вещества получили название блокаторов ионных каналов. Среди них лидокаин, новокаин, прокаин — вещества, при введении которых в организм в небольших дозах развивается блокада потенциапзависимых натриевых каналов нервных волокон и блокируется передача в ЦНС сигналов от болевых рецепторов. Эти вещества широко используются в медицинской практике в качестве местных обезболивающих средств.
Перемещение ионов через ионные каналы не только является основой перераспределения зарядов на мембранах и формирования электрических потенциалов, но и может оказывать влияние на протекание многих внутриклеточных процессов. Такое влияние на экспрессию генов, контролирующих синтез каналообразующих белков, не ограничено только клетками возбудимых тканей, но имеет место во всех клетках организма. Идентифицирована большая группа заболеваний, причиной которых является нарушение структуры и функции ионных каналов. Такие заболевания отнесены к группе «каналопатий». Очевидно, что знание строения и функций ионных каналов необходимо для понимания природы «каналопатий» и поиска их специфической терапии.
Лигандзависимые ионные каналы
Они обычно формируются белковыми макромолекулами, которые могут одновременно выполнять функцию ионных каналов и рецепторную функцию по отношению к определенным лигандам. Поскольку одна и та же макромолекула может одновременно выполнять эти две функции, то за ними закрепились разные названия — например, синаптический рецептор или лигандзависимый канал.
В отличие от потенциалзависимого ионного канала, открытие которого осуществляется при изменении конформации активационных ворот в условиях снижения трансмембранной разности потенциалов, лигандзависимые ионные каналы открываются (активируются) при взаимодействии пептидной (рецепторной) цепи белковой молекулы с лигандом — веществом, к которому рецептор имеет высокое сродство (рис. 4).

Рис. 4. Лигандзависимый ионный канал (никотинчувствительный ацетилхолиновый рецептор — н-ХР): а неактивный; 6 — активированный
Лигандзависимые ионные каналы обычно локализованы в постсинаптических мембранах нервных клеток и их отростков, а также мышечных волокон. Типичными примерами лигандзависимых ионных каналов являются каналы постсинаптических мембран, активируемые ацетилхолином (см. рис. 4), глутаматом, аспартатом, гамма-аминомасляной кислотой, глицином и другими синаптическими нейромедиаторами. Обычно название канала (рецептора) отражает тип нейро- медиатора, который в естественных условиях является его лигандом. Так, если это каналы нервно-мышечного синапса, в котором используется нейромедиатор ацетилхолин, то используется термин «ацетилхолиновый рецептор», а если он является к тому же чувствительным к никотину, то его называют никотинчувствительным, или просто н-ацетилхолиновым, рецептором (н-холинорецептор).
Обычно постсинаптические рецепторы (каналы) избирательно связываются только с одним типом нейромедиатора. В зависимости от типа и свойств взаимодействующих рецептора и нейромедиатора каналы избирательно изменяют свою проницаемость для минеральных ионов, но при этом они не являются строго селективными каналами. Например, лигандзависимые каналы могут изменять проницаемость для катионов Na+ и К+ или для К+ и анионов СI+. Такая избирательность связывания лиганда и изменения ионной проницаемости генетически закреплена в пространственной структуре макромолекулы.
Если взаимодействие медиатора и рецепторной части макромолекулы, формирующей ионный канал, непосредственно сопровождается изменением проницаемости канала, то в течение нескольких миллисекунд это приводит к изменению проницаемости постсинаптической мембраны для минеральных ионов и величины постсинаптического потенциала. Такие каналы названы быстрыми и локализуются, например, в постсинаптической мембране аксо-дендритных возбуждающих синапсов и аксосоматических тормозных синапсов.
Существуют медленные лигандзависимые ионные каналы. В отличие от быстрых каналов их открытие опосредованно не прямым взаимодействием нейромедиатора с макромолекулой- рецептором, а цепочкой событий, включающих активацию G-белка, его взаимодействие с GTP, повышение уровня вторичных посредников во внутриклеточной передаче сигнала нейромедиатора, которые, фосфорилируя ионный канал, приводят к изменению его проницаемости для минеральных ионов и соответствующему изменению величины постсинаптического потенциала. Вся описанная цепочка событий осуществляется уже за сотни миллисекунд. С такими медленными лигандзависимыми ионными каналами мы встретимся при изучении механизмов регуляции работы сердца, гладких мышц.
Особым типом являются каналы, локализованные в мембранах эндоплазматичсского ретикулума гладкомышечной клетки. Их лигандом является вторичный посредник внутриклеточной передачи сигнала инозитол-три-фосфат- ИФЗ.
Описаны ионные каналы, которые характеризуются некоторыми структурными и функциональными свойствами, присущими как потенциалзависимым, так и лигандзависимым ионным каналам. Они являются потенциалнечувствительными ионными каналами, состояние воротного механизма которых контролируется циклическими нуклеотидами (цАМФ и цГМФ). При этом циклические нуклеотиды связываются с внутриклеточной СООН-терминалыо каналообразующей молекулы белка и активируют канал.
Эти каналы характеризуются меньшей избирательностью проницаемости для катионов и способностью последних оказывать влияние на проницаемость друг друга. Так, ионы Са 2+ , поступая через активированные каналы из внеклеточной среды, блокируют проницаемость каналов для ионов Na 2+ . Одним из примеров таких каналов являются ионные каналы палочек сетчатки глаза, проницаемость которых для ионов Са 2+ и Na 2+ определяется уровнем цГМФ.
Лигандзависимые ионные каналы широко представлены в мембранных структурах, обеспечивающих синаптическую передачу сигналов от ряда сенсорных рецепторов в ЦНС; передачу сигналов в синапсах нервной системы; передачу сигналов нервной системы к эффекторным клеткам.
Уже отмечалось, что непосредственная передача команд нервной системы ко многим эффекторным органам осуществляется с помощью нейромедиаторов, активирующих лигандзависимые ионные каналы в постсинаптических мембранах. Однако их лигандами (агонистами или антагонистами) могут быть и вещества экзогенной природы, которые в ряде случаев используются в качестве лекарственных веществ.
Например, после введения в организм вещества диплацина, сходного по своей структуре с нейромедиатором апетилхолином, последует продолжительное открытие лигандзависимых ионных каналов нервно-мышечных синапсов, которые перестают передавать нервные импульсы с нервных волокон к мышцам. Наступает релаксация скелетных мышц организма, которая может понадобиться во время проведения сложных хирургических операций. Диплацин и другие вещества, способные изменять состояние лигандзависимых ионных каналов и блокировать передачу сигналов в нервно-мышечных синапсах, получили название миорелаксантов.

Рис. 5. Каналы щелевых контактов между двумя плотно контактирующими клетками
В медицинской практике используются многие другие лекарственные вещества, оказывающие влияние на состояние лигандзависимых ионных каналов клеток различных тканей.
Каналы щелевых (плотных) контактов клеток
Каналы щелевых контактов формируются в области контакта двух соседних клеток, очень близко прилежащих друг к другу. В мембране каждой контактирующей клетки шесть белковых субъединиц, получивших название коннексины, формируют гексагональную структуру, в центре которой образуется пора или ионный канал — коннексон (рис. 5).
Зеркальная структура образуется в месте контакта в мембране соседней клетки, и ионный канал между ними становится общим. Через такие ионные каналы из клетки в клетку могут перемещаться различные минеральные ионы, в том числе ионы Са 2+ , а также низкомолекулярные органические вещества. Каналы щелевых контактов клеток обеспечивают передачу информации между клетками миокарда, гладких мышц, сетчатки глаза, нервной системы.
Натриевые каналы
В клетках организма широко представлены потенциалзависимые, потенциалнезависимые (лигандзависимые, механочувствительные, пассивные и др.) натриевые каналы.
Потенциалзависимые натриевые каналы
Они состоят из одной а-субъединицы, формирующей канал, и двух β-субъединиц, модулирующих ионную проницаемость и кинетику инактивации натриевых каналов (рис. 6).

Рис. 6. Двухмерная структура а-субъединицы потенциал-зависимого натриевого канала. Описание в тексте
Как видно из рис. 6, а-субъединица представлена четырьмя однотипными доменами, состоящими из шести спирализованных трансмембранных сегментов, соединенных аминокислотными петлями. Петли, соединяющие 5-й и 6-й сегменты, окружают пору канала, а в составе 4-го сегмента содержатся положительно заряженные аминокислоты, которые являются сенсорами разности потенциалов на мембране и управляют положением воротного механизма при сдвигах трансмембранного потенциала.
В потенциалзависимых натриевых каналах имеются два воротных механизма, один из них — активационный (при участии 4-го сегмента) обеспечивает открытие (активацию) канала при деполяризации мембраны, а второй (при участии внутриклеточной петли между 3-м и 4-м доменами) — его инактивацию при перезарядке мембраны. Поскольку оба этих механизма быстро изменяют положение ворот канала, то потенциалзависимые натриевые каналы являются быстрыми ионными каналами и имеют определяющее значение для генерации потенциалов действия в возбудимых тканях и для их проведения по мембранам нервных и мышечных волокон.
Эти каналы локализуются в цитоплазматических мембранах аксонного холмика нейронов, в дендритах и аксонах, в мембране околосинаптичсской области нервно-мышечного синапса, в сарколемме волокон поперечно-полосатых мышц и сократительного миокарда. Плотность распределения натриевых каналов в этих структурах различна. В миелинизированных нервных волокнах они сосредоточены главным образом в области перехватов Ранвье, где их плотность достигает около 10 000 каналов на квадратный микрон площади, а в немиелинизированных волокнах каналы распределены более равномерно с плотностью около 20 каналов на ту же площадь. Эти каналы практически отсутствуют в структуре мембран тела нервной клетки, в мембране нервных окончаний, непосредственно формирующих сенсорные рецепторы, и в постсинаптических мембранах эффекторных клеток.
Среди потенциалзавиеимых натриевых каналов различают уже более девяти подтипов, отличающихся свойствами а-субъединиц, имеющих определенную тканевую принадлежность и отличающихся различной чувствительностью к действию блокаторов. Так, например, подтип канала, образованного каналообразующим белком, синтез которого контролируется геном SCN4A, имеется в сарколемме полностью дифференцированных и иннервированных скелетных мышц и его блокагорами являются тетродотоксин, сакситоксин и ц-конотоксины. В большинстве случаев а-субъединицы чувствительны к действию тетродотоксина, который в микромолярных концентрациях блокирует поры и тем самым вход в натриевые каналы.
Известны токсины натриевых каналов, вызывающие замедление скорости их инактивации. Например, токсин морской анемоны (АТХ) и а-токсин скорпиона (ScTX) вызывают замедление инактивации, связываясь с аминокислотными остатками петли S3-S4 4-го сегмента.
Синтезированы и широко используются в медицине для блокады быстрых потенциалзависимых натриевых каналов вещества, получившие название анестетиков (новокаин, дикаин, лидокаин, совкаин, прокаин и др.). Анестезия при блокаде ими натриевых каналов достигается за счет устранения возможности генерации нервных импульсов в афферентных нервных волокнах и тем самым блокады проведения сигналов от сенсорных болевых рецепторов в ЦНС.
Обнаружено, что изменение структуры натриевых каналов может вести к развитию ряда заболеваний. Так, например, изменение структуры канала, контролируемого геном SCNlb, ведет к развитию генерализованных форм эпилепсии и судорог при повышении температуры тела (фебрильных судорог).
Многие микроорганизмы образуют в организме человека токсины — вещества, под действием которых в поражаемых клетках блокируются ионные каналы, что может сопровождаться нарушением ионного баланса и гибелью клетки. Другие микроорганизмы, наоборот, своими токсинами (перфоринами) формируют в мембране клетки ионные каналы. В частности, токсин палочки сибирской язвы, вызывающей у человека особо опасную инфекцию, атакуя клетку, образует в ее мембране новые поры (каналы), через которые в клетку проникают другие токсины. Действием этих токсинов обусловлена гибель атакованных клеток и высокая смертность при этом заболевании. Учеными синтезировано вещество β-циклодекстрин, близкое по пространственной структуре к форме образующегося канала. Это вещество блокирует каналы, образуемые токсином микроорганизма, предотвращает поступление токсинов в клетки и спасает от гибели экспериментальных животных, зараженных палочкой сибирской язвы.
Потенциалнезависимые натриевые каналы
Лигандзависимые натриевые каналы. Их общее строение и свойства рассмотрены выше при описании лигандзависимых ионных каналов. Этот тип натриевых каналов широко представлен в организме натриевыми каналами никотинчувствительного холинорецептора постсинаптичсской мембраны нервно-мышечного синапса, межнейронных синапсов ЦНС и автономной нервной системы (преганглионарного и ганглионарного нейронов). Лигандзависимые натриевые каналы локализованы в постсинаптических мембранах других возбуждающих (глутамат- и аспартатергических) синапсов ЦНС. Они играют решающую роль в возникновении в синапсах возбуждающего постсинаптического потенциала и передаче сигналов между нейронами и между нейронами и эффекторными клетками.
Лигандзависимые натриевые каналы постсинаптической мембраны не являются строго селективными и могут быть проницаемы одновременно для нескольких ионов: натрия и калия, натрия и кальция.
Потенциалнезависимые натриевые каналы, управляемые вторичными посредниками. Состояние этих натриевых каналов может управляться с помощью цГМФ (фоторецеиторы), цАМФ (обонятельные рецепторы) и с помощью субъединиц G-белка (миокард).
Механочувствительные натриевые каналы. Представлены в механорецепторах стенок сосудов, сердца, полых внутренних органов, проприорсцепторах поперечно-полосатых мышц, мембране гладких миоцитов. С их участием в сенсорных рецепторах осуществляется преобразование энергии механического воздействия в колебание разности потенциалов — рецепторный потенциал.
Пассивные натриевые канаты. Содержатся в цитоплазма- тических мембранах возбудимых клеток. Проницаемость этих каналов для ионов Na+ небольшая, но через них ионы Na диффундируют по градиенту концентрации из внеклеточных пространств в клетки и несколько деполяризуют мембрану. Более существенно проницаемы в покос натриевые каналы цитоплазматической мембраны гладких миоцитов. Они деполяризуют ее на большую величину (потенциал покоя около 50 мВ), чем мембрану миоцитов поперечно-полосатой мускулатуры (потенциал покоя около 90 мВ). Таким образом, пассивные натриевые каналы участвуют в формировании мембранного потенциала покоя.
Натриевые обменники. Ранее был описан натрий-кальциевый обменный механизм, или натрий-кальциевый обменник, который играет важную роль в удалении ионов кальция из сократительных кардиомиоцитов.
Натрий-протонный обменник. Представляет собой особый тип каналообразующего белка, который удаляет протоны водорода из внутриклеточных пространств в обмен на поступление в клетку ионов натрия. Удаление протонов активируется при понижении в клетке рН.
Синтез белков, образующих обменные натриевые каналы, контролируется пятью генами, которые обозначаются как NAH1 -NAH5.
Калиевые каналы
Существуют потенциалзависимые и потенциалнечувствительные калиевые каналы. Среди последних выделяют пассивные, лигандзависимые и другие типы калиевых каналов. Как правило, калиевые каналы имеются в мембранах тех же клеток и тканей, в которых содержатся натриевые каналы. Одной из причин такого параллелизма в расположении этих ионных каналов является то, что ионы Na+ и К+ являются важнейшими катионами, от характера распределения и перемещения которых зависит возникновение и изменение электрических потенциалов как одной из важнейших форм передачи информационных сигналов в организме.
Существует целое суперсемейство калиевых ионных каналов, которые подразделяются но особенностям структуры, месту локализации и свойствам каналов на отдельные семейства, типы и подтипы. Описано более трех десятков калиевых каналов, и дать их подробную характеристику не представляется возможным. Поэтому в качестве примеров будут приведены описания тех семейств и типов ионных каналов, которые имеют отношение прежде всего к сигнальным путям и механизмам контроля нервных и мышечных процессов.
Пассивные калиевые каналы
Известно, что в состоянии покоя мембраны возбудимых клеток относительно хорошо проницаемы для ионов К и плохо для ионов Na+. Поскольку носителями трансмембранных электрических токов являются ионы, то, измеряя электрический ток, протекающий через мембрану клетки, можно судить о состоянии ионных каналов. Оказалось, что трансмембранный электрический ток, обусловленный диффузией ионов К по градиенту концентрации из клетки, составляет около двух пикоампер и имеет пульсирующий характер, а средняя продолжительность пульсации составляет несколько миллисекунд. Из этого наблюдения сделан вывод, что калиевые каналы в покоящейся клетке могут спонтанно открываться и закрываться, обеспечивая условия для диффузии через них ионов К из клетки и формирования на мембране потенциала покоя.
Потенциалзависимые калиевые каналы
О существовании потенциалзависимых калиевых каналов в мембранах клеток возбудимых тканей стало известно после того, как было установлено, что их кинетика активации отличается от таковой для потенциалзависимых натриевых каналов и к тому же они селективно блокируются другими блокаторами. Калиевые каналы активируются так же, как и натриевые, при деполяризации мембраны клетки до критического уровня, но при этом скорость выхода ионов К+ из клетки нарастает значительно медленнее, чем скорость входа ионов Na+ в клетку.
Селективный фильтр калиевого канала располагается с внутренней стороны устья поры в отличие от наружного расположения подобного фильтра в натриевых каналах (рис. 7). Существование селективности этих каналов по отношению к катионам Na+ и К+ и различных специфических блокаторов — тетродотоксина (для натрия) и тетраэтиламмония (для калия) — свидетельствует о различном строении этих каналов.
Потенциалзависимые калиевые каналы являются тетрамерами и состоят из четырех субъсдиниц, образующих пору в центре.
Потенциалзависимые калиевые каналы локализуются в мембранах как возбудимых, так и невозбудимых клеток. Они играют важную роль в скорости восстановления (реполяризации)потенциала на мембране после ее деполяризации и, таким образом, в контроле формы и частоты генерации потенциалов действия. Медленные калиевые каналы блокируются тстра- этиламмонием, 4-аминопиридином, фенциклидином, 9-аминоакридином.

Рис. 7. Калиевый канал: а — слева — двухмерная структура а-субъединицы; справа — схема канала; б — электроногра.мма калиевых каналов в цитопламатической мембране.
Кроме медленных калиевых каналов описаны быстрые потенциалзависимые калиевые каналы, кинетика открытия которых сходна с таковой для быстрых потенциалзависимых натриевых каналов. Эти калиевые каналы быстро открываются при деполяризации, затем полностью инактивируются, а для их реактивации требуется не просто реполяризовать мембрану, но на некоторое время гиперполяризовать ее.
В соответствии с названиями кодирующих синтез и сборку каналообразующих молекул генов выделяют шесть KCN типов с подтипами KCN А, В, С, Е и одно семейство KCNQ ионных каналов. Каналы последнего семейства экспрессированы в миокарде.
Лигандзависимые калиевые каналы
Представлены большим числом каналов, чувствительных к действию разнообразных лигандов.
Одним из типов многочисленных лигандзависимых калиевых каналов являются каналы, ассоциированные с мускаринчувствительными ацетилхолиновыми рецепторами. Эти каналы активируются ацетилхолином. Каналы могут блокироваться брадикинином и ионами бария. Есть два подтипа этих каналов: инактивирующиеся мускарином и активирующиеся им. Последний локализован в клетках водителя ритма сердца.
Свойствами лигандзависимого калиевого канала обладают неселективные потенциалнезависимые катионные каналы, сочетающие признаки каналов и никотинчувствительных ацетил холиновых рецепторов постсинаптической мембраны нервно-мышечного синапса. При взаимодействии белка-каналообразователя с ацетилхолином происходит открытие этого неселективного канала, через который ионы Na+ входят в мышечную клетку, а ионы К из нее выходят. Различная скорость перемещения этих ионов обеспечивает возникновение деполяризации постсинаптической мембраны, не перерастающей в потенциал действия непосредственно на этой мембране.
Выделены АТФ-чувствительные калиевые каналы, которые ингибируются и активируются действием АТФ.
Отдельное семейство калиевых каналов составляют так называемые входные выпрямляющие калиевые каналы (вентили), или входные выпрямители(inward rectifying ; inward rectifier ). В воротном механизме выпрямляющих калиевых каналов нет сенсора напряжения. Функциональное значение этих каналов состоит в их влиянии на возбудимость клеток-водителей ритма, мышечных клеток и нейронов.
Семейство выпрямляющих входных калиевых каналов в соответствии с названиями генов, их кодирующих, подразделяется более чем на 15 типов. Примером специфического значения выпрямляющих входных калиевых каналов и, в частности каналов KCNJ 3, 5, 6 и 9 (другое обозначение Kir-каналы) может быть их специфическая роль в регуляции частоты сердечных сокращении через ассоциацию этих каналов с G-белком и мускаринчувствительными ацетилхолиновыми рецепторами клеток — водителей ритма сердца.
Известны потенциалнечувствительные активируемые натрием калиевые каналы.
Описаны особые потенциалнечувствительные калиевые каналы, чувствительные к изменению рН, которые имеются в р-клетках островков поджелудочной железы и выполняют в них роль сенсора глюкозы. Известны также калиевые каналы, чувствительные к изменению объема клеток.
Кальциевые каналы
Семейство кальциевых каналов широко представлено в клетках нервной и мышечной тканей. Основными местами их локализации являются мембраны пресинаптических терминалей саркоплазматичсского и эндоплазматичсского ретикулума мышц, сарколеммы кардиомиоцитов и мембраны клеток других тканей.
Кальциевые каналы по способам управления проницаемостью подразделяют на потенциалзависимые, пассивные, лигандзависимые, механочувствительные и др.
Кальциевые каналы подразделяют по скорости инактивации на каналы Т-типа (transient — скоротечный), L-типа (медленные). В зависимости от тканевой принадлежности и чувствительности к действию токсинов выделяют каналы В-типа (brain — мозг), N-типа (neuronal — нейрональный), Р-типа (purkinje cell — клетка Пуркинье) и R-типа (резистентный к действию токсинов).
Потенциалзависимые кальциевые каналы
Они формируются олигомерным белком, обычно состоящим из пяти субъединиц а1, а2, β, у и δ. Собственно ионный канал формирует а-субъединица, имеющая большую степень сходства аминокислотного состава и структуры с аналогичной субъединицей потенциалзависимых натриевых и калиевых каналов (см. рис. 6, рис. 7).
Потенциалзависимый кальциевый канал обладает селективной проницаемостью для ионов Са 2+ . Селективность обеспечивается наличием поры, формирующей селективный фильтр.
Пора образована сегментами а 1 -субъединицы, поэтому, учитывая сходство се строения с таковой для каналов одновалентных катионов, следовало бы ожидать, что кальциевый канал должен быть проницаем для ионов Na+ и К+. Такое его свойство действительно имеет место при устранении кальция из внеклеточной среды.
В естественных условиях селективность по отношению к кальцию обеспечивается в канале наличием в поре канала двух мест связывания кальция. Одно из них образовано группой остатков глутамата, и при низкой концентрации кальция он оказывается сильно связанным с этим местом поры канала и канал для кальция становится слабо проницаемым. При повышении концентрации кальция возрастает вероятность занятия кальцием второго места связывания; возникающие при этом силы электростатического отталкивания между ионами Са 2+ сильно сокращают время пребывания ионов на местах связывания. Высвобождающийся кальций диффундирует через активированный канал в клетку по электрохимическому градиенту.
Потенциалзависимые кальциевые каналы различаются пороговыми значениями сдвигов разности потенциалов, при которых они активируются. Каналы Т-типа активируются малыми сдвигами напряжения на мембране, L- и Р-типов характеризуются высокими порогами сдвигов напряжениями, вызывающими их активацию.
Потенциалзависимые кальциевые каналы играют важную роль в осуществлении ряда жизненно важных процессов в организме. Их активация и поступление кальция в пресинаптическую терминаль являются необходимыми для осуществления синаптической передачи сигналов.
Вход кальция через кальциевые каналы в пейсмекерную клетку необходим для генерации потенциалов действия в клетках водителях ритма сердца и обеспечения его ритмического сокращения. Потенциалзависимые кальциевые каналы регулируют поступление кальция в саркоплазму волокон миокарда, скелетной мускулатуры, гладких миоцитов сосудов и внутренних органов, контролируя инициирование, скорость, силу, продолжительность их сокращения и тем самым движения, насосную функцию сердца, артериальное давление крови, дыхание и многие другие процессы в организме.
Пассивные кальциевые каналы
Имеются в цитоплазматических мембранах гладких миоцитов. Они проницаемы для кальция в состоянии покоя, и кальций наряду с ионами К+ и Na+ участвует в создании трансмембранной разности потенциалов или потенциала покоя гладких миоцитов. Кальций, поступающий по этим каналам в гладкий миоцит, является источником пополнения его запасов в эндоплазматическом ретикулуме, используется в качестве вторичного посредника при передаче внутриклеточных сигналов.
Кальций в состоянии покоя может перемещаться из клетки в клетку через каналы щелевых контактов. Эти каналы не являются селективными для кальция, и через них может одновременно осуществляться межклеточный обмен другими ионами и органическими веществами небольшой молекулярной массы. Кальций, поступающий в клетки через каналы щелевых контактов, играет важную роль в возникновении возбуждения, инициировании и синхронизации сокращений миокарда, матки, сфинктеров внутренних органов, поддержании тонуса сосудов.
Лигандзависимые кальциевые каналы
При изучении механизмов запуска и регуляции сокращений миокарда и гладких мыщц оказалось, что они зависят от поступления в мио- цит кальция как из внеклеточной среды, так и из его внутриклеточных хранилищ. При этом поступление кальция в саркоплазму может контролироваться изменением разности потенциалов на сарколемме и активацией потенциалзависимых кальциевых каналов и(или) действием на мембрану саркоплазматического ретикулума ряда сигнальных молекул.
Лигандзависимые кальциевые каналы локализованы в цитоплазматических мембранах гладких миоцитов. Лигандами их рецепторов могут выступать гормоны: вазопрессин, окситоцин, адреналин; нейромедиатор норадреналин; сигнальные молекулы: ангиотензин 2, эндотелии 1 и другие вещества. Связывание лиганда с рецептором сопровождается активацией кальциевого канала и входом кальция в клетку из внеклеточной среды.
В кардиомиоцитах для инициации мышечного сокращения необходимо первоначально активировать потенциалзависимые кальциевые каналы Т-типа, затем L-типа, открытие которых обеспечивает поступление в клетку некоторого количества ионов Са 2+ . Вошедший в клетку кальций активирует рианодиновый рецептор (RYR) каналообразующего белка, вмонтированного в мембране саркоплазматичсского ретикулума кардиомиоцита. В результате активации канала его проницаемость для кальция возрастает и последний по градиенту концентрации диффундирует в саркоплазму. Таким образом, ионы Са 2+ выступают в качестве своеобразных лигандов, активирующих рианодиновые рецепторы и тем самым кальциевые каналы. В результате входящий в клетку внеклеточный кальций выполняет роль триггера для выделения кальция из его основного внутриклеточного хранилища.
Кальциевые каналы могут одновременно проявлять чувствительность к изменениям разности потенциалов на цитоплазматической мембране и к действию лигандов. Например, L-тип потенциалзависимых кальциевых каналов чувствителен к дигидропиридину (нифедипину), фенилалкиламинам (верапамилу) и бензотиазепинам (дилтиазему). Этот тип каналов нередко называют дигидропиридиновыми рецепторами. Это название предполагает, что L-кальциевый канал является лигандзависимым, хотя в действительности он потен циалзависимый канал.
Р-тип каналов устойчив к действию коногоксинов и лекарств, к которым чувствительны другие типы кальциевых каналов.
Функциональные свойства а1,-субъединиц потенциалзависимых кальциевых каналов могут модулироваться при их фосфорилировании, и таким образом может регулироваться состояние ионной проницаемости кальциевых каналов, например, в миокарде.
Особым типом лигандзависимых ионных кальциевых каналов являются каналы, локализованные в мембранах эндоплазматического ретикулума гладкомышечной клетки, состояние проницаемости которых контролируется внутриклеточным уровнем вторичного посредника — ИФЗ. На примере этих каналов мы встречаемся со случаем, когда внеклеточная сигнальная молекула-агонист, активируя рецептор плазматической мембраны гладкомышечной клетки-мишени, включает инозитолфосфатный путь внутриклеточной передачи сигнала, который в свою очередь через действие ИФЗ выходит на активацию следующего каналообразующего белка в мембране органеллы клетки. Вся эта цепочка событий передачи сигнала завершается выходом из внутриклеточных депо ионов Са 2+ , запускающих и контролирующих молекулярный механизм сокращения гладкомышечной клетки.
Механочувствительные кальциевые каналы
Локализуются в плазматической мембране гладких миоцитов стенки сосудов, миоиитов внутренних органов, эндотелия сосудов, эпителия бронхов. Эти каналы могут быть ассоциированы с гликопротеиновыми механорецепторами. В ответ на механическое воздействие (например, растяжение стенки сосуда давлением крови) повышается проницаемость для ионов Са 2+ . Механочувствительные каналы не обладают высокой селективностью и изменяют их проницаемость одновременно для ряда катионов. Поступление в гладкомышечную клетку кальция и натрия вызывает деполяризацию ее мембраны, открытие потенциалзависимых кальциевых каналов, увеличение входа кальция и сокращение гладкого миоцита.
Эти события составляют часть механизма приспособления тонуса сосудов и регуляции кровотока к изменяющимся величинам давления крови в сосуде и скорости кровотока (миогенная регуляция). Кроме того, механочувствительные кальциевые каналы участвуют в реализации механизмов стресс-релаксации сосудов при длительном повышении давления крови.
Хлорные каналы
Хлорные каналы имеются в плазматических мембранах большинства клеток. Они играют важную роль в поддержании в покоящейся клетке трансмембранной разности потенциалов и их сдвигах при изменении функциональной активности клеток. Хлорные каналы участвуют в регуляции объема клеток, трансэпителиального переноса веществ, секреции жидкости секреторными клетками.
В соответствии с механизмами активации выделяют три суперсемейсгва хлорных каналов: потенциалзависимые, лигандзависимые и другие потенциалнечувствительные хлорные каналы.
Потенциал зависимые хлорные каналы. Локализуются в мембранах возбудимых и эпителиальных клеток. Состояние проницаемости этих каналов управляется величиной трансмембранной разности потенциалов.
Потенциал зависимая проницаемость хлорных каналов неодинакова в разных тканях. Так, в мембране аксонов зависимость проницаемости хлорных каналов от разности потенциалов незначительна и существенно не влияет на изменение величины потенциала действия при возбуждении, а в скелетных мышцах эта зависимость проницаемости хлорных каналов выше.
Канал CLC1 является типичным представителем хлорных каналов сарколеммы мышечного волокна скелетной мышцы. Канал проявляет проницаемость во всем диапазоне изменений трансмембранных напряжении в состоянии покоя, активируется при деполяризации и инактивируется при гиперполяризации мембраны.
Лигандзависимые хлорные каналы. Преимущественно экспрессируются в нервной ткани. Состояние проницаемости этих каналов для хлора управляется прежде всего внеклеточными лигандами, но они могут быть чувствительными к концентрации кальция внутри клетки, активироваться G-белками и цАМФ. Каналы этого типа широко распространены в пост- синаптических мембранах и используются для осуществления постсинаптического торможения. Управление состоянием проницаемости канала осуществляется путем активации каналов лигандами — тормозными нейромедиаторами (у-аминомасляной кислотой и глицином).
Потенциалнечувствительные хлорные каналы. Включают пассивные хлорные каналы, АТФ-чувствительные каналы и трансмембранный регулятор проводимости интерстициального фиброза (cystic fibrosis transmembrane conductance regulator — CFTR).
CFTR, по-видимому, состоит из собственно хлорного канала и канала-регулятора, представленного специальным регуляторным доменом (Р-доменом). Регуляция ионной проводимости этих каналов осуществляется путем фосфорилирования регуляторного домена цАМФ-зависимой протеинкиназой. Нарушение структуры и функции этого канала ведет к развитию тяжелого заболевания, сопровождаемого нарушением функции многих тканей — интерстициального фиброза.
Аквапорины
Аквапорины (от лат. aqua — вода, греч.porus — канал, пора) — белки, образующие водные каналы и обеспечивающие трансмембранный перенос воды. Аквапорины представлены интегральными, тетрамерными белками мембран, мономер которых имеет массу около 30 кДа. Таким образом, каждый аква- порин формирует четыре водных канала (рис. 8).
Особенностью этих каналов является то, что водные молекулы в них могут перемещаться в изоосмотических условиях, т.е. когда на них не действуют силы осмотического градиента. Для обозначения аквапоринов используется сокращение AQP. Выделен и описан ряд типов аквапоринов: AQP1 — в мембранах эпителия проксимальных почечных канальцев, нисходящем отделе петли Генле; в мембранах эндотелия и гладких миоцитов кровеносных сосудов, в структурах стекловидного тела; AQP2 — в мембранах эпителия собирательных трубок. Этот аквапорин оказался чувствительным к действию антидиуретического гормона, и на этом основании его можно рассматривать как лигандзависимый водный канал. Экспрессия гена, контролирующего синтез этого аквапорина, регулируется антидиуретическим гормоном; AQP3 обнаружен в мембранах клеток роговицы глаза; AQP4 — в клетках мозга.

Рис. 8. Структура водного канала AQP1: а — пептидные цепи, формирующие канал; б — канал в собранном виде: A, В, С, D, Е — участки белковой цепи
Оказалось, что AQP1 и AQP4 играют важную роль в образовании и циркуляции цереброспинальной жидкости. Аквапорины содержатся в эпителии желудочно-кишечного тракта: AQP4 — в желудке и тонкой кишке; AQP5 — в слюнных железах; AQP6 — в тонкой кишке и поджелудочной железе; AQP7 — в тонкой кишке; AQP8, AQP9 — в печени. Часть аквапоринов транспортирует не только молекулы воды, но и растворимые в ней вещества органической природы (кислород, глицерин, мочевина). Таким образом, аквапорины играют в организме важную роль в обмене воды и нарушение их функции может быть одной из причин формирования отеков мозга, легких и развития почечной и сердечной недостаточности.
Знание механизмов транспорта ионов через мембраны и способов влияния на этот транспорт является непременным условием не только для понимания механизмов регуляции жизненных функций, но и для правильного выбора лекарственных препаратов при лечении большого числа заболеваний (гипертонической болезни, бронхиальной астмы, сердечных аритмий, нарушений водно-солевого обмена и др.).
Для понимания механизмов регуляции физиологических процессов в организме необходимо знание не только структуры и проницаемости клеточных мембран для различных веществ, но и структуры и проницаемости более сложных структурных образовании, находящихся между кровью и тканями различных органов.
БИОЛОГИЧЕСКИЕ МЕМБРАНЫ И ИОННЫЕ КАНАЛЫ
Биологические мембраны – это функционально активные структуры клеток, ограничивающие цитоплазму и большинство внутриклеточных структур; образуют единую внутриклеточную систему канальцев, складок и замкнутых полостей.
Структурная основа мембраны – двойной слой фосфолипидов, в который встроены мембранные белки. Толщина клеточных мембран 6-12 нм. Молекулы липидов амфотерны. Своими гидрофильными частями они обращены в сторону водной среды (межклеточная жидкость и цитоплазма), гидрофобные части молекул направлены внутрь фосфолипидного бислоя. Такая структура идеально подходит для раздела внеклеточной и внутриклеточной фаз.
Белки, интегрированные в двойной слой фосфолипидов своими полярными участками, образуют гидрофильную поверхность в водной фазе. Они выполняют различные функции: рецепторную, ферментативную, образуют ионные каналы, являются мембранными насосами и переносчиками ионов и молекул.
Большинство наших знаний об устройстве ионного канала, является результатом функциональной реконструкции. Каждый канал имеет устье, селективный фильтр, ворота и механизм управления воротами.
Часть каналов являются электроуправляемыми, т.е. управляются за счет разности потенциалов на мембране (потенциал-зависимые ионные каналы). Для этого рядом с каналом имеется электрический сенсор, который в зависимости от величины мембранного потенциала либо открывает ворота каналов, либо держит их закрытыми.
Второй вариант ионных каналов – рецептороуправляемые. Ворота управляются за счет рецептора, расположенного на поверхности мембраны (открываются при взаимодействии медиатора с рецептором). В некоторых рецептороуправляемых каналах между рецептором и воротным механизмом имеется промежуточная стадия (посредник типа цАМФ, протеинкиназы и т.д.)
Ионные каналы обеспечивают два важных свойства мембраны: селективность и проводимость.
Селективность – или избирательность канала обеспечивается его особой белковой структурой, геометрией канала.
Например, диаметр иона натрия – 0,19 нм, вместе с гидратной оболочкой он становится около 0,3 нм. Устье натриевого канала 0,3 – 0,5 нм. Чтобы пройти через канал (особенно через селективный фильтр), ион натрия или другой ион должен освободиться от гидратной оболочки и только в «голом» виде может пройти через канал. Слишком большой ион не может войти в устье, слишком маленький не способен отдать гидратную оболочку в селективном фильтре, поэтому не может выскочить из канала.
Натриевые каналы (рис. 6) имеют ворота 2-х типов – активационные (m-ворота) и инактивационные (h-ворота). В условиях покоя активационные ворота закрыты, но готовы в любую минуту открыться, а инактивационные – открыты. При снижении МП (деполяризация до 60 мВ) активационные ворота открываются и впускают ионы натрия в клетку, но вскоре начинают закрываться инактивационные ворота (происходит инактивация натриевых каналов). Некоторое время спустя закрываются активационные ворота, открываются инактивационные, и канал готов к новому циклу. Канал блокируется тетродотоксином, местными анестетиками (новокаин и др.).
Рис. 6. Работа натриевых каналов и «воротных» механизмов.
А – в покое m-ворота закрыты; Б – при возбуждении m-ворота открыты; В – закрытие h-ворот (инактивация) при деполяризации.
Калиевые каналы тоже достаточно селективны – в основном пропускают ионы калия. Блокируются тетраэтиламмонием. Процессы инактивации у них выражены слабо. Зато имеются особые калиевые каналы, активирующиеся при повышении внутриклеточной концентрации кальция и деполяризации клеточной мембраны. Активация калий-калльцийзависимых каналов ускоряет реполяризацию (восстановление МП покоя).
Кальциевые каналы. Входящий кальциевый ток недостаточно велик, чтобы нормально деполяризовать клеточную мембрану. Кальций выступает в роли вторичного
посредника (мессенджера). Активация кальциевых каналов обеспечивается деполяризацией клеточной мембраны, напр., входящим натриевым током. Инактивация кальциевых каналов происходит при повышении внутриклеточной концентрации свободного кальция. Однако белки цитоплазмы связывают кальций, что позволяет некоторое время поддерживать стабильную величину кальциевого тока, хотя и на низком уровне; при этом натриевый ток полностью подавляется. Блокируются кальциевые каналы ионами марганца, никеля, кадмия (2-хвалентные ионы), а также лекарственными веществами (верапамил).
Различают пассивный (без затрат энергии) и активный (энергозависимый) транспорт ионов через мембраны.
Пассивный идет за счет простой и облегченной диффузии.
Простая диффузия идет в соответствии с законом Фика – по химическому, электрохимическому или осмотическому градиенту. Напр., в клетке натрия 14 ммоль, а в среде 140 ммоль, в этом случае пассивный поток должен быть направлен в клетку.
Для пассивной простой диффузии вещество должно быть жирорастворимым. Гидрофильные вещества в фосфолипидном бислое мембраны пройти не могут.
Облегченная диффузия происходит или при наличии специализированных каналов или с участием переносчиков, которые специфически связываются с переносимой молекулой, а затем способствуют ее переносу по градиенту концентрации.
Активный транспорт ионов насосами клеточных мембран обеспечивает поддержание ионных градиентов по обе стороны мембраны. Энергия затрачивается на перенос данного вещества против градиента его концентрации.
Доказано участие в активном транспорте ионов специализированных ферментных систем – АТФ-аз, которые осуществляют гидролиз АТФ. Различают:
Натрий–калиевая–АТФ–аза («натриевый насос») обнаружена в мембранах клеток всех животных, растений и микроорганизмов. Это мембранный белок, имеющий два центра связывания ионов. Один из них (натриевый) расположен на внутренней поверхности клеточной мембраны, второй (калиевый) – на ее внешней поверхности. Специфическим ингибитором фермента является сердечный гликозид – строфантин (уабаин), блокирующий работу натриевого насоса. Гидролиз одной молекулы АТФ сопровождается выведением из клетки трех ионов натрия и закачиванием в клетку двух ионов калия. При увеличении количества ионов калия во внеклеточной среде или ионов натрия внутри клетки работа насоса усиливается.
Кальциевая–АТФ-аза («кальциевый насос») наиболее широко распространена в мембранах саркоплазматического ретикулума мышечных клеток.
Протонная–АТФ-аза («протонный насос») – в мембранах митохондрий.