ការស្រូបយក
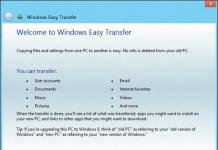
"H5N1" ដ៏ល្បីល្បាញតំណាងឱ្យ "hemagglutinin ប្រភេទទី 5, neuraminidase ប្រភេទទី 1" - ប្រូតេអ៊ីនទាំងពីរនេះនៅជាប់នឹងផ្ទៃនៃមេរោគគ្រុនផ្តាសាយ (ក្នុងរូបភាពទី 1 hemagglutinin មានពណ៌បៃតងហើយ neuraminidase មានពណ៌ប្រផេះ) ។
ដោយមានជំនួយពី hemagglutinin មេរោគគ្រុនផ្តាសាយភ្ជាប់ទៅនឹងអ្នកទទួលនៅលើផ្ទៃនៃកោសិកា។ គោលដៅដំបូងនៃមេរោគគឺកោសិកានៃ epithelium ciliated នៃផ្លូវដង្ហើម ប៉ុន្តែនេះមិនមែនជាមូលហេតុដែលយើងស្រឡាញ់វាទេ: hemagglutinin អាចភ្ជាប់ទៅនឹងអ្នកទទួលនៃកោសិកាផ្សេងទៀតជាច្រើនរួមទាំងកោសិកាឈាមក្រហម។ ប្រសិនបើមេរោគមួយជាប់នឹងកោសិកាឈាមក្រហមពីរ (ជាប់គ្នា) ក្នុងពេលតែមួយ កោសិកាឈាមក្រហមនឹងនៅជាប់គ្នា! ដូច្នេះឈ្មោះប្រូតេអ៊ីន - "ការកកឈាម" ។
អង្ករ។ ១
ការអនុវត្ត
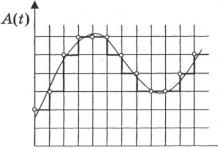
កោសិកាឆ្កួតស្រូបមេរោគដែលភ្ជាប់ខ្លួនវាទៅដោយ phagocytosis - ដូចជាបរិភោគវា។ ហេតុអ្វីបានជាក្មេងៗតែងតែដាក់របស់អាក្រក់គ្រប់ប្រភេទក្នុងមាត់?! ទោះជាយ៉ាងណាក៏ដោយ មេរោគនៅតែនៅខាងក្នុងកោសិកាជាអាហារ នៅខាងក្នុង phagocytic vesicle (ក្នុងរូបភាពទី 2 - "endosome")។ endosome បញ្ចូលគ្នាជាមួយ lysosome ដែលជា vacuole រំលាយអាហារត្រូវបានបង្កើតឡើង ប្រូតុងត្រូវបានបូមចូលទៅក្នុងវាពី cytoplasm ដើម្បីបង្កើតបរិយាកាសអាស៊ីត (ដំណើរការនេះត្រូវបានបង្ហាញក្នុងរូបភាពទី 2) - បន្តិចទៀត ហើយយើងនឹងរំលាយមេរោគ (ជាមួយ ពាក្យ “អាហារប្រូតេអ៊ីន តើមានអ្វីប្លែក”)។

អង្ករ។ ២
បន្ទះ
ប៉ុន្តែមេរោគបានត្រៀមរួចរាល់សម្រាប់វេននៃព្រឹត្តិការណ៍នេះ៖
 អង្ករ។ ៣ |
- Hemagglutinin ត្រូវបានកែប្រែក្រោមឥទិ្ធពលនៃបរិយាកាសអាស៊ីត - ផ្ទៃរបស់វាក្លាយទៅជាអ៊ីដ្រូហ្វីលីក ហើយវា (ពីមុនត្រូវបានភ្ជាប់ទៅឧបករណ៍ទទួលនៅលើផ្ទៃខាងក្នុងនៃភ្នាស endosome ឥឡូវនេះ) ត្រូវបានបង្កប់នៅក្នុងភ្នាសនេះ។
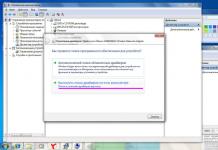
- ប្រូតុងដែលបូមចូលទៅក្នុង endosome ឆ្លងកាត់ប្រូតេអ៊ីនឆានែលពិសេស (ប្រូតេអ៊ីន M2 ដែលបង្ហាញក្នុងរូបភាពទី 1 និងរូបទី 3) តាមរយៈសែល lipid នៃមេរោគ ហើយទៅដល់សែលប្រូតេអ៊ីននៃមេរោគ (ក្នុងរូបភាពទី 1 - រង្វង់នៃគ្រាប់បាល់ពណ៌ស - ប្រូតេអ៊ីន M1) ។ ដោយសារតែនេះសែលប្រូតេអ៊ីនត្រូវបានបំផ្លាញ (ក្នុងរូបភាពទី 3 ប្រូតេអ៊ីន M1 នៃសែលប្រូតេអ៊ីនដែលត្រូវបានបំផ្លាញត្រូវបានចង្អុលបង្ហាញថាជាផ្កាយក្រហម) ។
- ស្រោមសំបុត្រ lipid នៃមេរោគ (ដោយសារតែសកម្មភាពជ្រៀតចូលនៃ hemagglutinin) ប្រសព្វជាមួយភ្នាស (lipid) នៃ phagosome; RNA នៃមេរោគបញ្ចប់នៅក្នុង cytoplasm នៃកោសិកា។
ការចម្លងមេរោគ
មេរោគ RNA ដែលបញ្ចេញទៅក្នុង cytoplasm គឺមានសុវត្ថិភាពទាំងស្រុង។
- ប្រូតេអ៊ីនមិនអាចត្រូវបានបង្កើតឡើងនៅលើវាទេព្រោះវាជាដក RNA (ប្រូតេអ៊ីនមិនត្រូវបានអ៊ិនកូដដោយវាទេប៉ុន្តែដោយខ្សែបូកដែលមិនទាន់មាន) ។
- វាក៏មិនអាចទៅរួចទេក្នុងការបង្កើត RNA នៅលើវា - កោសិការបស់យើងជាទូទៅមិនមានអង់ស៊ីមដែលមានសមត្ថភាពបង្កើន RNA ទ្វេដង។
“អូហូ-ហូ អ្នកមិនមានអ្វីទេ” មេរោគគ្រុនផ្តាសាយរអ៊ូរទាំដោយអង្រួនក្បាលពុកមាត់របស់គាត់ “ប៉ុន្តែមិនអីទេ ខ្ញុំបានយកអ្វីគ្រប់យ៉ាងមកជាមួយខ្ញុំ”។ មេរោគបាននាំមកជាមួយវានូវប្រូតេអ៊ីន PB1, PB2 និង PA ដែលរួមគ្នាបង្កើតបានជា RNA-dependent RNA polymerase របស់វីរុស - វាអាចចម្លង RNA ។ តែសំណាងអាក្រក់! វត្ថុធាតុ polymerase ណាមួយត្រូវការ primer ដើម្បីចាប់ផ្តើមដំណើរការ ប៉ុន្តែជំងឺផ្តាសាយភ្លេចមិនបានយកវាទៅជាមួយទេ! ចប់ហើយ?!
ស្ងប់ស្ងាត់កុំភ័យ! - ជាមួយនឹងពាក្យទាំងនេះក្រុមហ៊ុនទាំងមូល (8 មេរោគ RNAs និង 3 អង់ស៊ីមមេរោគ) ត្រូវបានបញ្ជូនទៅស្នូលកោសិកា។ នៅទីនោះជំងឺគ្រុនផ្តាសាយទទួលបានសេវាកម្មពេញលេញ៖
- primers សម្រាប់ការចម្លង RNA មេរោគ (ដើម្បីទទួលបាន RNA បូក) គឺជាផ្នែកដែលកាត់ចេញពី RNA កោសិកា។
- ដំណើរការ៖ តំបន់ដែលបានបម្រើការជាបឋមសម្រាប់ការសំយោគ RNA - ទាំងនេះគឺជាមួក ដូច្នេះការកែប្រែនៃចុង 5" ត្រូវបានអនុវត្តនៅដើមដំបូង; នៅចុងបញ្ចប់នៃការសំយោគ polyadelation នៃចុង 3" កើតឡើង។
- splicing: មេរោគ RNA មួយចំនួនដែលមានព័ត៌មានសម្រាប់ប្រូតេអ៊ីនពីរត្រូវបានកាត់ជាពីរផ្នែក។
នៅក្នុងវិធីនេះ បូក RNAs ត្រូវបានសំយោគ ដែលអាចបម្រើជាគំរូសម្រាប់ការសំយោគប្រូតេអ៊ីនមេរោគ និង RNAs ដកមេរោគ។
បន្ទាប់មកអ្វីគ្រប់យ៉ាងគឺសាមញ្ញ: កោសិកាល្ងង់ដោយប្រើ ribosomes របស់វាពីអាស៊ីតអាមីណូផ្ទាល់របស់វាសំយោគប្រូតេអ៊ីននៃវីរុសរួមទាំង RNA polymerase ដែលពឹងផ្អែកលើ RNA ។ Influenza minus RNA ក៏ត្រូវបានផលិតយ៉ាងខ្លាំងក្លានៅខាងក្នុងស្នូលផងដែរ។ ការប្រមូលផ្តុំនៃភាគល្អិតមេរោគកើតឡើងនៅក្នុង cytoplasm នៅលើផ្ទៃខាងក្នុងនៃភ្នាសកោសិកា។ មេរោគដែលបានបញ្ចប់ចាកចេញពីកោសិកាដោយ exocytosis (budding) neuraminidase ខាំខ្សែស្រឡាយចុងក្រោយដែលភ្ជាប់កោសិកានិងមេរោគដែលទើបនឹងកើត ... ជីវិតតូចមួយ (អាក្រក់) ថ្មីចេញមកក្នុងពិភពលោក!

អង្ករ។ ៤
ជំងឺគ្រុនផ្តាសាយ IRISES៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍
D.K. Lvov, A.D. Zaberezhny, T.I. អាលីភើរ
លោក Dmitry Konstantinovich Lvov អ្នកសិក្សានៃបណ្ឌិត្យសភាវិទ្យាសាស្ត្រវេជ្ជសាស្ត្ររុស្ស៊ី នាយកវិទ្យាស្ថានស្រាវជ្រាវមេរោគ បានដាក់ឈ្មោះតាម។ ឌី. Ivanovsky RAMS, ប្រធាននាយកដ្ឋានមេរោគ, បណ្ឌិតសភាវេជ្ជសាស្ត្រម៉ូស្គូបានដាក់ឈ្មោះតាម។ ពួកគេ។ Sechenov ។ អ្នកគ្រប់គ្រងគម្រោង 05-04-52136, 06-04-48822។
Alexey Dmitrievich Zaberezhny, បណ្ឌិតវិទ្យាសាស្ត្រជីវសាស្រ្ត, ប្រធានមន្ទីរពិសោធន៍នៃការធ្វើរោគវិនិច្ឆ័យម៉ូលេគុលនៃវិទ្យាស្ថានដូចគ្នា, ប្រធាននាយកដ្ឋានជីវវិទ្យាម៉ូលេគុលនៃ NPO Narvak ។
Taras Ivanovich Aliper, បណ្ឌិតវិទ្យាសាស្ត្រជីវសាស្រ្ត, ប្រធានមន្ទីរពិសោធន៍នៃមធ្យោបាយការពារជាក់លាក់នៃជំងឺមេរោគនៃវិទ្យាស្ថានដូចគ្នា, នាយក NPO Narvak ។
សម្រាប់ការបោះពុម្ពដំបូងនៃអត្ថបទ សូមមើល៖ ធម្មជាតិ។ 2006. លេខ 6 ។ ទំព័រ ៣–១៣។
ជំងឺគ្រុនផ្តាសាយកើតមានជារៀងរាល់ឆ្នាំ ហើយមិនត្រូវបានគេយល់ថាជាអ្វីដែលអស្ចារ្យនោះទេ។ ដោយសារជំងឺនេះបង្កឡើងដោយមេរោគដែលស៊ាំនឹងប្រព័ន្ធភាពស៊ាំ។
តាមក្បួនមួយគាត់ស៊ូទ្រាំនឹងពួកគេ។ ជំងឺរាតត្បាតគឺជាបញ្ហាមួយទៀត៖ ក្នុងករណីនេះ ភ្នាក់ងារបង្កជំងឺគ្រុនផ្តាសាយគឺជាមេរោគដែលមានលក្ខណៈសម្បត្តិ antigenic និងជីវសាស្រ្តថ្មី រីករាលដាលយ៉ាងឆាប់រហ័សពាសពេញពិភពលោក ដែលប៉ះពាល់ដល់មនុស្សរហូតដល់មួយភាគបួននៃចំនួនប្រជាជននៃភពផែនដី និងទាមទារជីវិតរាប់សិបលាននាក់។ នេះគឺជាអ្វីដែលធ្វើឱ្យជំងឺរាតត្បាតនៃសតវត្សចុងក្រោយនេះល្បីល្បាញ។ វាមិនអាចទៅរួចទេក្នុងការមើលជាមុនពួកគេដូចជាវាមិនអាចទៅរួចទេក្នុងការដាក់ឈ្មោះពេលវេលាពិតប្រាកដនៃការចាប់ផ្តើមនៃថ្មីមួយ។
ទោះជាយ៉ាងណាក៏ដោយ ឥឡូវនេះ ដោយសារការតាមដានជាប្រចាំនៃមេរោគដែលកំពុងចរាចរក្នុងចំណោមមនុស្ស សត្វក្នុងស្រុក និងសត្វព្រៃ ក៏ដូចជាចំណេះដឹងដែលទទួលបានដោយប្រើវិធីសាស្ត្រហ្សែនម៉ូលេគុល វាអាចទៅរួចរួចហើយដើម្បីទស្សន៍ទាយការលេចឡើងនៃវ៉ារ្យ៉ង់មេរោគថ្មីដែលមាននិន្នាការរាតត្បាត។ ក្នុងរយៈពេលប៉ុន្មានឆ្នាំចុងក្រោយនេះ បេក្ខជនសម្រាប់តួនាទីនេះត្រូវបានគេកំណត់អត្តសញ្ញាណ៖ ដំបូងឡើយវីរុស H5N1 មិនបង្ករោគនៅចុងបញ្ចប់នៃឆ្នាំ 2003 បណ្តាលឱ្យមានការរីករាលដាលនៃជំងឺគ្រុនផ្តាសាយក្នុងចំណោមសត្វបក្សី ដែលប្រែទៅជា panzootic នៅឆ្នាំនេះ។ មេរោគនេះបានចាប់ផ្ដើមឆ្លងដល់សត្វដទៃទៀត រួមទាំងមនុស្ស ប៉ុន្តែមិនទាន់អាចចម្លងពីមនុស្សទៅមនុស្សបាននៅឡើយទេ។ ដើម្បីឱ្យវាទទួលបានសមត្ថភាពនេះ វាគ្រប់គ្រាន់ដើម្បីជំនួសអាស៊ីតអាមីណូតែមួយនៅក្នុងប្រូតេអ៊ីនមេរោគមួយ។
រចនាសម្ព័ន្ធ Virion
រចនាសម្ព័ន្ធនៃមេរោគគ្រុនផ្តាសាយគឺសាមញ្ញណាស់៖ វាគឺជាភាគល្អិតស្វ៊ែរ (virion) ដែលមានអង្កត់ផ្ចិតប្រហែល 0.13 មីក្រូន ក្នុងស្នូលដែលមាន nucleocapsid (ម៉ូលេគុល RNA ខ្ចប់ក្នុងសែលប្រូតេអ៊ីន M1) ព័ទ្ធជុំវិញដោយ ភ្នាស lipid (រូបភាពទី 1) ។ ប្រូតេអ៊ីនបីត្រូវបានជ្រមុជនៅក្នុងភ្នាសនេះ - hemagglutinin, neuraminidase និងឆានែលអ៊ីយ៉ុង (ប្រូតេអ៊ីន M2) ដែលដើរតួយ៉ាងសំខាន់ក្នុងដំណើរការឆ្លង។
Hemagglutinin គឺជាអ្នកដំបូងដែលចូលមកទាក់ទងជាមួយអ្នកទទួលកោសិកាម៉ាស៊ីន។ នៅលើផ្ទៃនៃស្រោមសំបុត្រមេរោគត្រូវបានបង្ហាញនៅក្នុងទម្រង់នៃ trimers ស្មុគស្មាញបំផុត។ ម៉ូណូមឺរនីមួយៗរបស់ពួកគេត្រូវបានបោះយុថ្កាយ៉ាងរឹងមាំនៅក្នុងភ្នាស ហើយមានផ្នែករងពីរ - មួយក្នុងចំនោមពួកវាធានានូវទំនាក់ទំនងបឋមជាមួយកោសិកាគោលដៅ មួយទៀតគឺទទួលខុសត្រូវចំពោះការលាយបញ្ចូលគ្នានៃភ្នាសមេរោគ និងកោសិកា។ នៅផ្នែកខាងលើនៃប្រូតេអ៊ីនមានតំបន់ដែលភ្ជាប់ទៅនឹងអាស៊ីត sialic ដែលជាផ្នែកមួយនៃអ្នកទទួលកោសិកាម៉ាស៊ីន។
អង់ស៊ីម neuraminidase បំបែកចេញពីក្រុមអាស៊ីត sialic ស្ថានីយរបស់អ្នកទទួលកោសិកា ដែលជាលទ្ធផលដែលកោសិកាបាត់បង់សមត្ថភាពក្នុងការទទួលស្គាល់អង់ទីហ្សែន ហើយមេរោគបានជ្រាបចូល។

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
ចូលទៅក្នុងវាតាមរយៈ endocytosis ដែលជាវិធីសាស្រ្តទូទៅនៃការបញ្ជូនសារធាតុចូលទៅក្នុងកោសិកា។ បរិយាកាសអាសុីតនៃស្រទាប់ endosome ចេញពីភ្នាសកោសិកាធ្វើឱ្យឆានែលអ៊ីយ៉ុង M2 សកម្មដែលបន្ថយ pH នៅខាងក្នុងភាគល្អិតមេរោគដែលនាំទៅដល់ការបំផ្លាញសែលប្រូតេអ៊ីន M1 ។ ក្នុងពេលជាមួយគ្នានេះ hemagglutinin ត្រូវបានធ្វើឱ្យសកម្ម។ វាត្រូវបានសំយោគក្នុងទម្រង់ជាមុនគេ ដែលនៅក្នុងបរិយាកាសអាសុីតឆ្លងចូលទៅក្នុងសភាពចាស់ទុំ - វាត្រូវបានបំបែកដោយអង់ស៊ីម proteolytic ទៅជាពីររង ខណៈពេលដែល fusion peptide ដែលលាក់នៅខាងក្នុង trimer ផ្លាស់ប្តូរការអនុលោមភាពត្រូវបានបញ្ចេញ ផ្លាស់ទីទៅចុងខាងលើ។ នៃម៉ូលេគុល និងត្រូវបានបញ្ចូលទៅក្នុងភ្នាស។ ស្រោមសំបុត្រមេរោគបញ្ចូលគ្នាជាមួយ endosomal មួយ រន្ធ fusion ត្រូវបានបង្កើតឡើង ដែលតាមរយៈនោះផ្លូវមួយបើកចូលទៅក្នុង cytoplasm សម្រាប់សម្ភារៈហ្សែនបរទេស។ បន្ទាប់មក RNA មេរោគចូលទៅក្នុងស្នូលកោសិកា។ ជាលទ្ធផល ដំណើរការសំខាន់ៗរបស់កោសិកាត្រូវបានរំខាន ហើយកោសិកាខ្លួនឯង ដោយប្រើធនធានផ្ទាល់ខ្លួន ចាប់ផ្តើមផលិតប្រូតេអ៊ីនមេរោគ។ ភ្លាមៗ ការចម្លង RNA របស់មេរោគកើតឡើង ហើយភាគល្អិតមេរោគថ្មីត្រូវបានប្រមូលផ្តុំ ដែលដោយមានជំនួយពី neuraminidase ត្រូវបានបញ្ចេញចេញពីកោសិកាដែលខូច (ផលិតផលបំបែករបស់វាបណ្តាលឱ្យមានការពុលដល់រាងកាយ និងស្ថានភាព febrile) និងរាលដាលពាសពេញរាងកាយតាមរយៈចរន្តឈាម។
រូបភាពទី 1. ដ្យាក្រាមនៃមេរោគគ្រុនផ្តាសាយ virion ។ សែល lipoprotein របស់វាត្រូវបានគ្របដណ្តប់ដោយឆ្អឹងខ្នងនៃ glycoproteins ពីរ - hemagglutinin និង neuraminidase ។ នៅខាងក្នុងមាន nucleocapsid - ម៉ូលេគុល RNA ខ្ចប់នៅក្នុងសែលនៃប្រូតេអ៊ីន M1 ។ ហ្សែននេះមានបំណែកចំនួនប្រាំបី ដែលក្នុងនោះប្រាំមួយដំបូងបានអ៊ិនកូដប្រូតេអ៊ីនមួយនីមួយៗ (hemagglutinin - HA, neuraminidase - NA, RNA polymerase subunits - PB1, PB2, PA, nucleoprotein
NP) និងហ្សែនពីរចុងក្រោយ - ប្រូតេអ៊ីនពីរដែលនីមួយៗមានលំដាប់អាមីណូតែមួយគត់
noacids (ប្រូតេអ៊ីនម៉ាទ្រីស - M1, M2 និងប្រូតេអ៊ីនដែលមិនមានរចនាសម្ព័ន្ធ - HS1, HS2) ។
មេរោគច្រើនរារាំងប្រព័ន្ធ hematopoietic និងប្រព័ន្ធភាពស៊ាំ បំផ្លាញ endothelium នៃ capillaries ដែលនាំឱ្យមានការកើនឡើងនូវភាពជ្រាបចូលនៃសរសៃឈាម និងការហូរឈាម រួមទាំងការហើមខួរក្បាលជាមួយនឹងលទ្ធផលធ្ងន់ធ្ងរ។ ប៉ុន្តែរឿងនេះកើតឡើងកម្រណាស់ ជាធម្មតាប្រព័ន្ធភាពស៊ាំបើក - ដំបូងកត្តានៃភាពស៊ាំពីខាងក្នុង (មិនជាក់លាក់) ត្រូវបានពាក់ព័ន្ធ ហើយបន្ទាប់ពីមួយរយៈពេលអង្គបដិប្រាណជាក់លាក់ចាប់ផ្តើមត្រូវបានផលិត ដែលបញ្ចេញពួកវា ហើយនៅពេលឆ្លងឡើងវិញ ការពាររាងកាយ។ ពីមេរោគ។
លក្ខណៈពិសេសប្លែកនៃមេរោគគ្រុនផ្តាសាយគឺភាពប្រែប្រួលខ្ពស់នៃលក្ខណៈសម្បត្តិអង់ទីហ្សែន។ ប្រូតេអ៊ីនខាងក្នុងគឺថេរនៅក្នុងរចនាសម្ព័ន្ធរបស់វាហើយកំណត់ប្រភេទនៃមេរោគ (A, B និង C) ។ ផ្ទុយមកវិញ អង់ទីហ្សែនលើផ្ទៃគឺខុសគ្នា និងប្រែប្រួល និងច្រើនទៀត

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
នេះក៏អនុវត្តចំពោះ hemagglutinin (H) ដែលរួមជាមួយនឹង neuraminidase (N) កំណត់ប្រភេទរងនៃមេរោគ (H1N1, H2N2, H3N2 ។ល។)។ ភាពប្រែប្រួលនៃអង់ទីហ្សែននៃប្រូតេអ៊ីនលើផ្ទៃគឺបណ្តាលមកពីដំណើរការហ្សែនពីរ - ការរសាត់ និងការផ្លាស់ប្តូរការផ្លាស់ប្តូរនៅក្នុងហ្សែនមេរោគ។
ការផ្លាស់ប្តូររសាត់ត្រូវបានបង្កឡើងដោយការផ្លាស់ប្តូរចំណុចនៅក្នុងហ្សែនដែលបានអ៊ិនកូដ hemagglutinin និង neuraminidase ហើយនាំឱ្យមានការផ្លាស់ប្តូរតិចតួចនៅក្នុងរចនាសម្ព័ន្ធនៃប្រូតេអ៊ីនទាំងនេះ។ ជាធម្មតា ការផ្លាស់ប្តូរបែបនេះកើតឡើងរវាងជំងឺរាតត្បាតចំពោះមេរោគគ្រប់ប្រភេទ (A, B និង C)។ ជាលទ្ធផល ជំងឺរាតត្បាតជាជាងជំងឺរាតត្បាតកើតឡើងជារៀងរាល់ឆ្នាំ ចាប់តាំងពីការការពារពីការប៉ះពាល់ពីមុនជាមួយវីរុសនៅតែមាន ទោះបីជាវាមិនគ្រប់គ្រាន់ក៏ដោយ។
ការផ្លាស់ប្តូរការផ្លាស់ប្តូរកើតឡើងបន្ទាប់ពីការជំនួសហ្សែនពេញលេញ។ នេះគឺអាចធ្វើទៅបានចាប់តាំងពីហ្សែននៃមេរោគគ្រុនផ្តាសាយត្រូវបានបែងចែក - វាមានប្រាំបីបំណែកនៃ RNA លីនេអ៊ែរតែមួយខ្សែ ការអ៊ិនកូដ បន្ថែមលើ hemagglutinin និង neuraminidase ដែលជាអង់ស៊ីមជាក់លាក់នៃមេរោគ (RNA polymerase ឬ transcriptase ដែលមានបីរង។ - ប្រូតេអ៊ីន PB1, PB2, PA) ក៏ដូចជា nucleoprotein (NP), ម៉ាទ្រីស (M1 និង M2) និងប្រូតេអ៊ីន nonstructural (NS1 និង NS2) ។ នៅពេលដែលកោសិកាមួយត្រូវបានឆ្លងមេរោគក្នុងពេលដំណាលគ្នាដោយពីរប្រភេទផ្សេងគ្នានោះ ផ្នែកនៃហ្សែនចម្លងរបស់ពួកវាត្រូវបានលាយបញ្ចូលគ្នានៅក្នុងការរួមបញ្ចូលគ្នាណាមួយ ដូច្នេះ virion ថ្មីមានសំណុំហ្សែនផ្សេងៗគ្នាដែលខ្ចីពីមេរោគដើមនីមួយៗ។ ការរួមបញ្ចូលគ្នានៃផ្នែក RNA មេរោគនេះត្រូវបានគេហៅថា ការសាប់ហ្សែន ឬការចាត់ថ្នាក់ឡើងវិញ ដើម្បីកុំឱ្យមានការភ័ន្តច្រឡំជាមួយនឹងពាក្យដែលមានស្រាប់ - ការផ្សំឡើងវិញ ក្នុងអំឡុងពេលដែលសម្ភារៈហ្សែនត្រូវបានរៀបចំឡើងវិញដោយយន្តការឆ្លងកាត់ ឬជាលទ្ធផលនៃការផ្លាស់ប្តូរនៅក្នុង គំរូ។ ការផ្លាស់ប្តូរការផ្លាស់ប្តូរ, ជាក្បួន, ប៉ះពាល់ដល់រចនាសម្ព័ន្ធ antigenic នៃ hemagglutinin, តិចជាញឹកញាប់ - neuraminidase ។ ដូច្នេះនៅចន្លោះពេលមិនទៀងទាត់ (10-40 ឆ្នាំ) មេរោគដែលមានលក្ខណៈសម្បត្តិ antigenic និងជីវសាស្រ្តថ្មីលេចឡើង រួមទាំងវ៉ារ្យ៉ង់ជំងឺរាតត្បាតថ្មី។
របាំងនៃប្រភេទសត្វ
ក្នុងចំណោមមេរោគដែលអាចបង្កឱ្យមានស្ថានភាពអាសន្នរោគ ការប្រយុទ្ធប្រឆាំងនឹងការដែលនៅដំណាក់កាលនៃការកើតឡើងរបស់ពួកគេគឺពិបាកឬសូម្បីតែមិនអាចទៅរួចនោះ មេរោគគ្រុនផ្តាសាយ A គឺមានគ្រោះថ្នាក់ជាពិសេសពួកគេត្រូវបានកំណត់លក្ខណៈដោយភាពដូចគ្នានៃអង់ទីហ្សែនខ្ពស់នៃប្រូតេអ៊ីនលើផ្ទៃ ហើយត្រូវបានតំណាង នាមត្រកូលដោយ 16 ប្រភេទរង hemagglutinin (H1-16) និង 9 neuraminidase (N1-9) ។ មេរោគទាំងនេះរីករាលដាលនៅក្នុងធម្មជាតិ ហើយអាចឆ្លងដល់ប្រភេទសត្វស្លាបទាំងអស់ និងប្រភេទថនិកសត្វមួយចំនួន (មនុស្ស សេះ ជ្រូក ត្រីបាឡែន សត្វផ្សោត។ល។)។ ការឆ្លងនៃថនិកសត្វកើតឡើងជាចម្បងតាមរយៈផ្លូវដង្ហើមនិងនៅក្នុងបក្សី - តាមរយៈពោះវៀន។ ការឆ្លងរបស់ពួកគេជាធម្មតាមិនមានរោគសញ្ញា ឬក្នុងទម្រង់នៃជំងឺរលាកពោះវៀនធំ ដែលបង្ហាញពីកម្រិតខ្ពស់នៃការសម្របខ្លួនទៅវិញទៅមកនៃមេរោគគ្រុនផ្តាសាយ និងបក្សីព្រៃ ដែលអាចចាត់ទុកថាជាម្ចាស់ផ្ទះធម្មជាតិរបស់ពួកគេ។ មេរោគនៅតែមាននៅក្នុងទឹកនៅសីតុណ្ហភាព +22°C - រហូតដល់មួយខែនៅ +4°C និងខាងក្រោម - រយៈពេលយូរជាងនេះ (6-8 ខែ) ដូច្នេះផ្លូវទឹក - លាមកនៃការឆ្លងគឺជាយន្តការចម្បងសម្រាប់ការថែរក្សា។ ចរាចរជាប្រចាំនៃមេរោគគ្រុនផ្តាសាយនៅក្នុងធម្មជាតិ។
ថ្វីបើមានភាពតំណពូជនៃអង់ទីហ្សែនក៏ដោយ មេរោគដែលមានការរួមផ្សំនៃប្រូតេអ៊ីនលើផ្ទៃដែលគេស្គាល់ទាំងអស់ត្រូវបានញែកចេញពីសត្វស្លាបព្រៃនៃស្មុគស្មាញក្នុងទឹក និងពាក់កណ្តាលទឹក - ទា សត្វក្រៀល។ល។ (រូបទី 2) ។
មានតែមេរោគដែលមានសំណុំប្រូតេអ៊ីនលើផ្ទៃជាក់លាក់មួយប៉ុណ្ណោះដែលចរាចរក្នុងចំណោមសត្វដទៃទៀត៖ ឧទាហរណ៍ រហូតមកដល់ពេលថ្មីៗនេះ មេរោគនៃប្រភេទរង hemagglutinin បីប្រភេទ (H1-H3) និងប្រភេទរង neuraminidase ពីរ (N1-N2) ត្រូវបានញែកដាច់ពីមនុស្ស។ ជំងឺរាតត្បាតទាំងបួននៃសតវត្សទី 20 ។ ត្រូវបានបង្កឡើងដោយការផ្លាស់ប្តូរថ្មីនៃប្រភេទរងទាំងនេះ៖ "ជំងឺគ្រុនផ្តាសាយអេស្ប៉ាញ" ក្នុងឆ្នាំ 1918 ត្រូវបានបង្កឡើងដោយវីរុសផ្តាសាយ A នៃប្រភេទរង H1N1 "ជំងឺគ្រុនផ្តាសាយអាស៊ី" ក្នុងឆ្នាំ 1957 - H2N2 "ជំងឺគ្រុនផ្តាសាយហុងកុង" ក្នុងឆ្នាំ 1968 - H3N2 និង "ជំងឺគ្រុនផ្តាសាយរុស្ស៊ី" ក្នុងឆ្នាំ 1977 - H1N1 ។ ពួកវាទាំងអស់សុទ្ធតែជាអ្នកធានាឡើងវិញនៃមេរោគគ្រុនផ្តាសាយបក្សី និងមនុស្ស។

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
រហូតមកដល់ពេលថ្មីៗនេះ វាត្រូវបានគេជឿថា មេរោគគ្រុនផ្តាសាយបក្សី មិនមែនជាមេរោគសម្រាប់មនុស្សទេ ហើយប្រសិនបើឆ្លងមេរោគ អាចបណ្តាលឱ្យមានជំងឺរលាកស្រោមខួរ និងជំងឺគ្រុនផ្តាសាយស្រាល ហើយក្នុងករណីកម្រ រោគសញ្ញាផ្លូវដង្ហើមស្រាល។ ទោះជាយ៉ាងណាក៏ដោយ ក្នុងឆ្នាំ 1997 មេរោគ H5N1 បានបង្កជាទម្រង់ជំងឺធ្ងន់ធ្ងរបំផុតក្នុងចំណោមប្រជាជននៅទីក្រុងហុងកុង - ក្នុងចំណោមមនុស្ស 18 នាក់បានឈឺ 6 នាក់បានស្លាប់ ពួកគេទាំងអស់បានឆ្លងពីសត្វមាន់។ វគ្គស្រដៀងគ្នាទីពីរបានកើតឡើងនៅក្នុងខែកុម្ភៈ ឆ្នាំ 2003 ផងដែរនៅក្នុងទីក្រុងហុងកុង - ក្នុងចំណោមអ្នកឆ្លងទាំងប្រាំនាក់ ពីរនាក់បានស្លាប់។ មេរោគ H5N1 ត្រូវបានដាក់ឱ្យនៅដាច់ដោយឡែកពីសត្វមាន់ និងប្រភេទបក្សីផ្សេងទៀត (រួមទាំងសត្វព្រៃ) ក្នុងប្រជាជនក្នុងតំបន់។
រូប ២. គ្រោងការណ៍នៃការចរាចរនៃប្រភេទរងនៃមេរោគគ្រុនផ្តាសាយ A ដែលគេស្គាល់។
មេរោគ H9N2 serotype ដែលរីករាលដាលក្នុងចំណោមបសុបក្សីនៅក្នុងប្រទេសចិន និងបណ្តាប្រទេសអាស៊ីផ្សេងទៀត ត្រូវបានរកឃើញនៅក្នុងប្រជាជនចិន 5 នាក់ក្នុងខែសីហា ឆ្នាំ 1998 ហើយមួយឆ្នាំក្រោយមកនៅក្នុងទីក្រុងហុងកុងចំពោះក្មេងស្រីពីរនាក់ដែលមានរូបភាពគ្លីនិកនៃជំងឺផ្តាសាយ។ គួរកត់សម្គាល់ថាករណីជំងឺទាំងអស់កើតឡើងដោយឯករាជ្យពីគ្នាទៅវិញទៅមក ហើយមិនមានការចម្លងមេរោគពីមនុស្សទៅមនុស្សនោះទេ។ នៅឆ្នាំ 1996 មេរោគផ្តាសាយបក្សី H7N7 ត្រូវបានញែកដាច់ពីស្ត្រីម្នាក់ដែលមានជំងឺរលាកស្រោមខួរ។ ករណីមួយនៅប្រទេសហូឡង់ បណ្តាលឲ្យស្លាប់។ ទាំងនេះគ្រាន់តែជាករណីដែលត្រូវបានកត់ត្រាជាផ្លូវការប៉ុណ្ណោះ តាមការពិត មេរោគគ្រុនផ្តាសាយបក្សីបានយកឈ្នះលើរបាំងនៃប្រភេទសត្វ ជាក់ស្តែងកាន់តែញឹកញាប់ ហើយចាប់ផ្តើមឆ្លងមិនត្រឹមតែមនុស្សប៉ុណ្ណោះទេ ប៉ុន្តែក៏មានសត្វដទៃទៀតដែរ (ជ្រូក សេះ ត្រីបាឡែន មីង ជាដើម)។ . មានករណីឆ្លងជំងឺបក្សី (មាន់ ទួរគី) ដែលមានមេរោគគ្រុនផ្តាសាយ ជាលក្ខណៈសត្វស្លាបព្រៃ ជាពិសេសសត្វស្លាប។
វានៅតែពិបាកក្នុងការវិនិច្ឆ័យដោយទំនុកចិត្តលើកត្តាទាំងអស់ដែលកំណត់ជួរម៉ាស៊ីននៃមេរោគ និងយន្តការដែលមានឥទ្ធិពលលើការផ្លាស់ប្តូរម៉ាស៊ីន។ ការស្វែងរកនេះត្រូវបានដំណើរការអស់មួយរយៈមកហើយ នៅក្នុងក្រុមស្រាវជ្រាវផ្សេងៗ រួមទាំងនៅវិទ្យាស្ថានរបស់យើង។
Hemagglutinin គឺជាអ្នកដំបូងដែលស្ថិតក្រោមការសង្ស័យ ព្រោះវាជា glycoprotein នេះដែលទទួលខុសត្រូវក្នុងការទទួលស្គាល់អ្នកទទួលកោសិកាម៉ាស៊ីន និងចូលរួមក្នុងការលាយបញ្ចូលគ្នានៃស្រោមសំបុត្រមេរោគជាមួយនឹងស្រោមសំបុត្រ endosomal (សំខាន់គឺជាផ្នែកមួយនៃស្រោមសំបុត្រ cytoplasmic នៃកោសិកាម៉ាស៊ីន)។ រចនាសម្ព័នរបស់អ្នកទទួលទាំងនេះខុសគ្នាអាស្រ័យលើប្រភេទ និងប្រភពដើមនៃកោសិកា។ ភាពខុសគ្នាទាំងនេះមានសារៈសំខាន់សម្រាប់កំណត់ការផ្លាស់ប្តូរនៃមេរោគរវាងប្រភេទសត្វ ហើយត្រូវបានសិក្សាជាពិសេសទាក់ទងនឹងការលេចឡើងនៃមេរោគរាតត្បាតថ្មីរបស់មនុស្ស។
វាត្រូវបានបង្កើតឡើងថាអ្នកទទួលនៃកោសិកា epithelial នៃផ្លូវដង្ហើមរបស់មនុស្សបន្ថែមពីលើប្រូតេអ៊ីនមានផ្ទុកកាបូអ៊ីដ្រាត - sialo-oligosaccharides ដែលក្នុងនោះអាស៊ីត sialic ស្ថានីយ (N-acetylneuraminic acid) ត្រូវបានភ្ជាប់ទៅនឹង galactose ដោយ 2′-6 ។ ចំណង និងអ្នកទទួលកោសិកា

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
epithelium ពោះវៀនសត្វ - 2'-3' ។ មេរោគគ្រុនផ្តាសាយបក្សីបន្តពូជមិនល្អនៅក្នុងខ្លួនមនុស្ស ព្រោះវាមិនអាចទាក់ទងអ្នកទទួលរបស់មនុស្សបានទេ។ ក្នុងពេលជាមួយគ្នានេះ mucins (តាមធម្មជាតិនៃ glycoproteins ស្មុគស្មាញដូចគ្នាជាមួយនឹងអាស៊ីត sialic នៅចុងបញ្ចប់) ដែលមានកាតព្វកិច្ចការពារសួតរបស់មនុស្សពីអតិសុខុមប្រាណមានអ្នកទទួលជាមួយនឹងចំណង 2′-3′ galactose ។ ដូច្នេះ មេរោគគ្រុនផ្តាសាយបក្សីដែលចូលក្នុងខ្លួនមនុស្សដោយចៃដន្យ មិនអាចជ្រាបចូលទៅក្នុងកោសិកាបានទេ ដោយសារមិនមានអ្នកទទួលជាក់លាក់ណាមួយនៅលើផ្ទៃរបស់វា ហើយសកម្មភាពទទួលស្គាល់ virion receptors ត្រូវបានរារាំងដោយ mucin ដូច្នេះមនុស្សម្នាក់ក្នុងករណីនេះប្រឈមមុខនឹងការហៀរសំបោរបន្តិចប៉ុណ្ណោះ។ .
ប៉ុន្តែក្នុងករណីនេះ តើយើងអាចពន្យល់ពីការកើតឡើងនៃការប្រែប្រួលនៃការឆ្លងរាលដាលនៃមេរោគដោយរបៀបណា? ស្ថានភាពកាន់តែច្បាស់បន្តិច នៅពេលដែលគេដឹងថា កោសិកាផ្លូវដង្ហើមជ្រូកផ្ទុកអ្នកទទួលទាំងពីរប្រភេទ ហើយតាមនោះ អាចឆ្លងដោយមេរោគគ្រុនផ្តាសាយទាំងមនុស្ស និងសត្វបក្សី។ នេះមានន័យថាសត្វជ្រូកអាចមានសក្តានុពលធ្វើជាម្ចាស់ផ្ទះកម្រិតមធ្យមសម្រាប់មេរោគផ្សេងៗគ្នា និងជាសង្វៀនដ៏ល្អសម្រាប់ការចាត់ថ្នាក់របស់ពួកគេឡើងវិញក្នុងអំឡុងពេលមានការឆ្លងមេរោគចម្រុះ។
ចំពោះ hemagglutinin សមត្ថភាពរបស់វាក្នុងការទទួលស្គាល់អ្នកទទួលកោសិការបស់ម៉ាស៊ីនហាក់ដូចជាទាក់ទងជាចម្បងទៅនឹងរចនាសម្ព័ន្ធនៃកន្លែងភ្ជាប់អ្នកទទួល (RBS) ។ ដូច្នេះនៅក្នុងមេរោគគ្រុនផ្តាសាយរបស់មនុស្ស PCC មានអាស៊ីតអាមីណូ leucine និង serine នៅទីតាំង 226 និង 228 រៀងគ្នា ហើយនៅក្នុងមេរោគបក្សី glutamine និង glycine ត្រូវបានរកឃើញនៅក្នុងមុខតំណែងទាំងនេះ។ ការជំនួសអាស៊ីតអាមីណូផ្សេងទៀតត្រូវបានគេរកឃើញនៅក្នុង PCC នៅក្នុងសត្វផ្សេងៗគ្នា មានន័យថាទោះបីជា PCC ត្រូវបានអភិរក្ស និងមានការវិវត្តន៍មានស្ថេរភាពក៏ដោយ វានៅតែមានតំបន់ប្រែប្រួលដែលប៉ះពាល់ដល់ការភ្ជាប់អ្នកទទួល (ភាពស្និទ្ធស្នាល) និងភាពជាក់លាក់។
ជាឧទាហរណ៍ PCC អាចផ្លាស់ប្តូរបានបន្ទាប់ពីមេរោគបានយកឈ្នះលើរបាំងអន្តរប្រភេទ។ ភស្តុតាងដែលថារបាំងប្រភេទសត្វបក្សីអាចយកឈ្នះបានគឺការផ្ទុះឡើងនៃជំងឺផ្តាសាយមនុស្សឆ្នាំ 1997 នៅហុងកុងដែលបណ្តាលមកពីវីរុស H5N1 ។
វាត្រូវបានគេសន្មត់ថា "ការភ្ជាប់" នៃមេរោគទៅនឹងម៉ាស៊ីនត្រូវបានកំណត់មិនត្រឹមតែដោយលក្ខណៈនៃ hemagglutinin ប៉ុណ្ណោះទេប៉ុន្តែថែមទាំងដោយប្រូតេអ៊ីនផ្ទៃផ្សេងទៀត - neuraminidase ។ លើសពីនេះទៀត មានហេតុផលដើម្បីជឿថាហ្សែននៃប្រូតេអ៊ីនខាងក្នុង និងមិនមានរចនាសម្ព័ន្ធនៃមេរោគគ្រុនផ្តាសាយ A មានជាប់ពាក់ព័ន្ធក្នុងការកំណត់ជួរនៃម៉ាស៊ីន ទោះជាយ៉ាងណាក៏ដោយ វាលឿនពេកក្នុងការនិយាយអំពីរឿងនេះ ព្រោះវានៅតែចាំបាច់ក្នុងការសិក្សាការរួមចំណែករបស់ ហ្សែននីមួយៗ និងមុខងារនៃផលិតផលរបស់ពួកគេ។ ទោះជាយ៉ាងណាក៏ដោយ វាជាការសំខាន់ណាស់ដែលត្រូវយល់ថា សូម្បីតែការផ្លាស់ប្តូរតិចតួចបំផុតនៅក្នុងរចនាសម្ព័ន្ធនៃប្រូតេអ៊ីនមេរោគ ជាពិសេស hemagglutinin អាចនាំឱ្យមានការផ្លាស់ប្តូរយ៉ាងសំខាន់មិនត្រឹមតែនៅក្នុងជួរម៉ាស៊ីននៃមេរោគប៉ុណ្ណោះទេ ប៉ុន្តែថែមទាំងកម្រិតនៃការបង្កជំងឺរបស់វា (មេរោគ) ផងដែរ។
មេរោគ
ចូរយើងចាំថាសម្រាប់ការបន្តពូជនៃមេរោគនៅក្នុងរាងកាយម្ចាស់ផ្ទះ ការធ្វើឱ្យសកម្មនៃមុនគេនៃម៉ូលេគុល hemagglutinin គឺចាំបាច់ ហើយវាត្រូវបានបំបែកដោយ host proteases ទៅជាពីររង។ Proteolysis នៃ hemagglutinins នៃមេរោគបង្កជំងឺទាបកើតឡើងក្នុងចំនួនកោសិកាមានកំណត់ ដូច្នេះមេរោគត្រូវបានធ្វើមូលដ្ឋានីយកម្មតែនៅក្នុងផ្លូវដង្ហើម ឬពោះវៀនប៉ុណ្ណោះ។ វាកើតឡើងជាមួយនឹងការឆ្លងមេរោគ asymptomatic ឬកម្រិតមធ្យម។ Hemagglutinins នៃមេរោគបក្សីដែលបង្កជំងឺខ្លាំងត្រូវបានបង្ខូចនៅក្នុងកោសិកាផ្សេងៗ ហើយដូច្នេះវាមានសមត្ថភាពបង្ករោគជាប្រព័ន្ធដ៍សាហាវ ជាពិសេសនៅក្នុងបសុបក្សី។
មន្ទីរពិសោធន៍ជាច្រើននៅជុំវិញពិភពលោកបានចាប់ផ្តើមសិក្សាអំពីហ្សែននៃមេរោគគ្រុនផ្តាសាយដែលបង្កជំងឺខ្លាំងចំពោះមនុស្ស (H5N1 និង H7N7 ដាច់ដោយឡែកក្នុងឆ្នាំ 1997-2004)។ វាបានប្រែក្លាយថាមេរោគទាំងនេះមានអាស៊ីតអាមីណូមូលដ្ឋានជាច្រើននៅកន្លែងបំបែកនៃម៉ូលេគុល hemagglutinin ដែលផ្តល់ឱ្យពួកគេនូវសកម្មភាពឆ្លងខ្ពស់ និងបង្កជំងឺ។ មិនដូចមេរោគដែលមិនបង្កជំងឺ ឬមេរោគខ្សោយ ដែលមិនមានលំដាប់អាស៊ីតអាមីណូនេះទេ ហេម៉ាហ្គាគ្លូទីនីននៃមេរោគបង្កជំងឺខ្ពស់ត្រូវបានសម្អាតយ៉ាងងាយមិនត្រឹមតែដោយសារធាតុប្រូតេអុីនដូច trypsin ដែលមាននៅក្នុងកោសិកានៃផ្លូវដង្ហើមមនុស្ស និងពោះវៀនរបស់បក្សីប៉ុណ្ណោះទេ។ ផងដែរដោយ proteases ដូច furin ។ ពួកគេធ្វើសកម្មភាពរួមគ្នា

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
ជាមួយ ubiquitin ដែលត្រូវបានរចនាឡើងដើម្បីសម្គាល់ប្រូតេអ៊ីនដែលត្រូវការបំផ្លាញសម្រាប់ proteases ។ Proteases ដូច Furin ត្រូវបានសំយោគនៅក្នុងជាលិកាផ្សេងៗគ្នា ដែលផ្តល់ឱ្យមេរោគបង្កជំងឺនូវសមត្ថភាពក្នុងការឆ្លងប្រព័ន្ធ និងសរីរាង្គផ្សេងៗ។ ដើម្បីបំប្លែងមេរោគដែលបង្កជំងឺទាបទៅជាមេរោគបង្កជំងឺខ្លាំង ការបញ្ចូលអាស៊ីតអាមីណូមូលដ្ឋានសូម្បីតែមួយទៅក្នុងកន្លែងបំបែក proteolytic នៃ hemagglutinin គឺគ្រប់គ្រាន់ហើយ។
នេះត្រូវបានបញ្ជាក់ជាបន្តបន្ទាប់នៅក្នុងការពិសោធន៍លើសត្វកណ្តុរដែលឆ្លងមេរោគ H5N1 ប្រភេទផ្សេងគ្នា (ដាច់ដោយឡែកក្នុងឆ្នាំផ្សេងគ្នា)។ ពួកវាខ្លះចាប់ផ្តើមចម្លងនៅក្នុងខួរក្បាល ថ្លើម លំពែង និងកោសិកាឈាម ដែលបណ្តាលឱ្យសត្វកណ្តុរស្លាប់ 100% នៅថ្ងៃទី 7 ដល់ទី 8 បន្ទាប់ពីឆ្លងមេរោគ ខណៈមេរោគផ្សេងទៀតប្រែទៅជាមិនបង្កជំងឺសម្រាប់សត្វកណ្តុរ ហើយកើនឡើងតែនៅក្នុង សួត។ នេះត្រូវបានពន្យល់ភ្លាមៗ - នៅក្នុងមេរោគ H5N1 ដាច់ដោយឡែកក្នុងឆ្នាំ 2004 ក្នុងការប្រៀបធៀបជាមួយនឹងមេរោគដែលទទួលបានក្នុងឆ្នាំ 1997-2003 ការផ្លាស់ប្តូរបន្ថែមនៅក្នុងហ្សែន hemagglutinin ត្រូវបានគេកំណត់អត្តសញ្ញាណដែលប៉ះពាល់ដល់ការផ្លាស់ប្តូរលក្ខណៈសម្បត្តិអង់ទីហ្សែនរបស់ពួកគេ។
ភ្នាក់ងារបង្កជំងឺនៃមេរោគអាចត្រូវបានប៉ះពាល់ដោយការផ្លាស់ប្តូររចនាសម្ព័ន្ធនៃផ្ទៃមិនត្រឹមតែប៉ុណ្ណោះទេប៉ុន្តែថែមទាំងប្រូតេអ៊ីនខាងក្នុងផងដែរ។ ដូច្នេះការផ្លាស់ប្តូរមួយត្រូវបានគេរកឃើញនៅទីតាំង 627 នៅក្នុងប្រូតេអ៊ីន PB2 នៅក្នុងប្រភេទវីរុសផ្តាសាយ H5N1 ដែលជាភ្នាក់ងារបង្ករោគខ្ពស់សម្រាប់សត្វកណ្តុរ។ វាគឺជាការផ្លាស់ប្តូរនេះដែលមានឥទ្ធិពលលើភាពខុសគ្នានៃលក្ខណៈសម្បត្តិនៃមេរោគ H5N1 ពីរដែលនៅដាច់ដោយឡែកពីគេក្នុងទីក្រុងហុងកុង ហើយជាលទ្ធផល លទ្ធផលនៃដំណើរការឆ្លង។ លើសពីនេះ ភាពសាហាវនៃមេរោគគ្រុនផ្តាសាយទាំងនេះត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងលក្ខណៈរចនាសម្ព័ន្ធនៃប្រូតេអ៊ីន NS ដែលមិនមានរចនាសម្ព័ន្ធ ជាពិសេសជាមួយនឹងវត្តមានអាស៊ីត glutamic នៅក្នុងម៉ូលេគុលរបស់វានៅទីតាំង 92 ដែលធ្វើឱ្យមេរោគមានភាពធន់នឹងសកម្មភាពប្រឆាំងមេរោគរបស់ interferons ។ .
ជាការពិតណាស់ ការប្រើប្រាស់វិធីសាស្ត្រហ្សែនម៉ូលេគុលទំនើបក្នុងការសិក្សាអំពីមេរោគគ្រុនផ្តាសាយកំពុងបញ្ជាក់អំពីលក្ខណៈជីវសាស្រ្តរបស់វាបន្តិចម្តងៗ ប៉ុន្តែវិធីសាស្ត្របែបបុរាណដែលតាមដានចរាចរនៃមេរោគគ្រុនផ្តាសាយក្នុងចំនោមមនុស្ស សត្វក្នុងស្រុក និងសត្វព្រៃមិនសំខាន់នោះទេ។ ការទស្សន៍ទាយការលេចឡើងនៃភ្នាក់ងារបង្ករោគដែលមាននិន្នាការរាតត្បាត និងការបង្កើតវិធានការប្រកបដោយប្រសិទ្ធភាពសម្រាប់ការបង្ការ និងគ្រប់គ្រងជំងឺគ្រុនផ្តាសាយអាចត្រូវបានបង្កើតឡើងដោយផ្អែកលើការសិក្សាអំពីបរិស្ថានវិទ្យា និងការវិវត្តន៍នៃមេរោគដែលពិបាកព្យាករណ៍ និងពិបាកក្នុងការគ្រប់គ្រងជំងឺឆ្លងនេះ។ ការស្រាវជ្រាវបែបនេះបានចាប់ផ្តើមជាង 35 ឆ្នាំមុនដោយ G. Laver នៅប្រទេសអូស្ត្រាលី R. Webster នៅសហរដ្ឋអាមេរិក D.K. Lvov នៅក្នុងប្រទេសរបស់យើងហើយពួកគេបន្តរហូតដល់សព្វថ្ងៃនេះនៅទូទាំងពិភពលោក។
ព្រឹត្តិការណ៍ និងការព្យាករណ៍
ការសិក្សាដ៏ទូលំទូលាយនៃមេរោគគ្រុនផ្តាសាយ A ត្រូវបានផ្តួចផ្តើមដោយអង្គការសុខភាពពិភពលោក (WHO) បន្ទាប់ពីជំងឺរាតត្បាតឆ្នាំ 1968 ដែលបណ្តាលមកពីវីរុស H3N2 ។ វិទ្យាស្ថានរបស់យើងបានបង្កើតឡើងថា បុព្វបុរសនៃ H3N2 គឺជាប្រភេទមេរោគដែលស្រដៀងទៅនឹងមេរោគ H3N8 ដែលនៅដាច់ពីគេក្នុងប្រទេសអ៊ុយក្រែនក្នុងឆ្នាំ 1963 ពីសត្វទាព្រៃ។ ទិន្នន័យទាំងនេះ និងទិន្នន័យផ្សេងទៀតបានបម្រើជាមូលដ្ឋានសម្រាប់ការអភិវឌ្ឍនៃទិសដៅវិទ្យាសាស្ត្រ - បរិស្ថានវិទ្យា និងការវិវត្តនៃមេរោគគ្រុនផ្តាសាយ A មជ្ឈមណ្ឌលជាតិសម្រាប់បរិស្ថានវិទ្យានៃមេរោគគ្រុនផ្តាសាយ A ត្រូវបានបង្កើតឡើងជាមួយនឹងបណ្តាញនៃមូលដ្ឋានគាំទ្រ ដែលទិន្នន័យថ្មីត្រូវបានគេទទួលបាននោះ។ បានបញ្ជាក់ពីអវត្តមាននៃភាពខុសគ្នាជាមូលដ្ឋានរវាងមេរោគគ្រុនផ្តាសាយ A របស់មនុស្ស និងសត្វ ពោលគឺ .e.e. វត្តមាននៃបណ្តុំហ្សែនការពារតែមួយ។ យោងតាមទិន្នន័យទាំងនេះនៅឆ្នាំ 1980 ចំណាត់ថ្នាក់នៃមេរោគគ្រុនផ្តាសាយត្រូវបានបង្កើតឡើងដោយមិនគិតពីប្រភពដើមរបស់វា។ ចាប់តាំងពីពេលនោះមក មេរោគដាច់ដោយឡែកនីមួយៗត្រូវបានផ្តល់ឈ្មោះ ដែលឆ្លុះបញ្ចាំងពីប្រភេទនៃមេរោគ ប្រភពនៃភាពឯកោ ទីកន្លែង និងឆ្នាំនៃភាពឯកោ ក៏ដូចជាប្រភេទរង - ឧទាហរណ៍ A/duck/Ukraine/63(H3N8)។
គោលបំណងសំខាន់នៃការស្រាវជ្រាវរបស់យើងនៅក្នុងប្រទេសរុស្ស៊ីគឺដើម្បីសិក្សាពីការវិវត្តនៃមេរោគគ្រុនផ្តាសាយ A នៅក្នុងដំណើរការនៃអន្តរកម្មនៃចំនួនមេរោគជាមួយនឹងចំនួនសត្វបក្សីព្រៃ និងសត្វក្នុងស្រុក និងការបង្កើតប្រភេទសត្វដែលមានសក្តានុពលនៃការរីករាលដាល។ ចំពោះគោលបំណងនេះ ការត្រួតពិនិត្យត្រូវបានអនុវត្តនៅចំណុចសំខាន់ៗនៅអឺរ៉ាស៊ីខាងជើង។ មេរោគ 14 ក្នុងចំណោម 16 ដែលគេស្គាល់ត្រូវបានញែកដាច់ពីគេ
នៅចុងឆ្នាំ 2003 i.e. បីខែមុនការផ្ទុះឡើងនៃការរាតត្បាតដែលបង្កឡើងដោយមេរោគផ្តាសាយបក្សី H5N1 នៅក្នុងបណ្តាប្រទេសនៃអាស៊ីអាគ្នេយ៍ អ្នកនិពន្ធម្នាក់នៃអត្ថបទនេះ (D.K. Lvov) បាននិយាយនៅឯសមាជជំងឺគ្រុនផ្តាសាយអន្តរជាតិក្នុងប្រទេសជប៉ុនដោយរាយការណ៍ពីភាពឯកោនៃមេរោគទាំងនេះ។

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
ពីបក្សីព្រៃនៅប្រទេសរុស្ស៊ី - នៅ Altai និងនៅភាគខាងត្បូងនៃ Primorye ។ យោងតាមទិន្នន័យហ្សែនម៉ូលេគុលប្រភេទទាំងនេះត្រូវបានចាត់ថ្នាក់ជាភ្នាក់ងារបង្កជំងឺទាប។ បន្ទាប់មក ដោយភាពស្រដៀងគ្នាជាមួយនឹងការសង្កេតពីមុន ការទស្សន៍ទាយដំបូងត្រូវបានធ្វើឡើងអំពីលទ្ធភាពនៃការណែនាំរបស់ពួកវាជាមួយសត្វស្លាបដែលធ្វើចំណាកស្រុកទៅក្នុងកសិដ្ឋានបសុបក្សីនៅអាស៊ីអាគ្នេយ៍ ដែលបន្ទាប់ពីពេលខ្លះពួកវាអាចប្រែទៅជាបង្កជំងឺខ្លាំងជាមួយនឹងសក្តានុពលនៃជំងឺរាតត្បាត និងជំងឺរាតត្បាត។ ជាក់ស្តែងនេះគឺជាអ្វីដែលបានកើតឡើង។ ការផ្ទុះឡើងនៃជំងឺអេពីហ្សូទីកបានរីករាលដាលដល់១០ប្រទេសក្នុងរយៈពេលដ៏ខ្លី ។ ក្នុងរយៈពេលកន្លងមក មាន់ និងទាជាង 150 លានក្បាលបានងាប់ និងត្រូវបានសម្លាប់។ យោងតាមអង្គការសុខភាពពិភពលោក គិតត្រឹមដំណាច់ខែមីនា ឆ្នាំ២០០៦ មនុស្ស១៨៥នាក់បានឆ្លងមេរោគរួចហើយ ក្នុងនោះ១០៤នាក់បានស្លាប់។ ការរាតត្បាតនៅតែបន្ត ហើយមេរោគក៏បានជ្រាបចូលទៅក្នុងហ្វូងជ្រូកផងដែរ ដែលជាការគួរឱ្យព្រួយបារម្ភជាពិសេស។ ពិភពលោកអាចឈានដល់ដំណាក់កាលនៃគ្រោះមហន្តរាយរាតត្បាត៖ អ្នកធានាអាចបង្កើតបានគ្រប់ពេលវេលានៅពេលដែលជ្រូកត្រូវបានឆ្លងមេរោគ H5 ក្នុងពេលដំណាលគ្នា និងវីរុសផ្តាសាយមនុស្ស H1 ឬ H3 ដែលចរាចរពាសពេញពិភពលោក។
ការព្យាករណ៍ទីពីរក៏ត្រូវបានធ្វើឡើងផងដែរ៖ ប្រសិនបើសត្វស្លាបព្រៃត្រូវបានឆ្លងមេរោគដែលមានមេរោគខ្លាំងនៅក្នុងតំបន់រដូវរងា ហានិភ័យនៃការណែនាំរបស់វាទៅក្នុងប្រទេសរុស្ស៊ីកើនឡើង ជាពិសេសនៅស៊ីបេរី និងចុងបូព៌ា ក្នុងអំឡុងពេលធ្វើចំណាកស្រុកនៅនិទាឃរដូវ។ ហើយបន្ទាប់មកអ្វីដែលសន្មត់ថានឹងកើតឡើង។ នៅពាក់កណ្តាលខែកក្កដាឆ្នាំ 2005 នៅក្នុងតំបន់ដែលមានប្រជាជននៃតំបន់ Novosibirsk ដែលមានទីតាំងនៅភាគខាងជើង lacustrine ព្រៃ steppe នៃ Baraba Lowland, epizootic ក្នុងចំណោមសត្វបក្សីត្រូវបានរកឃើញជាមួយនឹងអត្រាមរណភាពជាង 90% និងការរីករាលដាលយ៉ាងឆាប់រហ័ស។
សម្ភារៈត្រូវបានប្រមូលពីសត្វស្លាបក្នុងស្រុក និងសត្វព្រៃដែលរស់នៅក្នុងតំបន់ជុំវិញតំបន់អេពីហ្សូទិក។ ដោយប្រើខ្សែកោសិកា SPEV និង MDCK (វិធីសាស្ត្រមិនធម្មតានេះបច្ចុប្បន្នកំពុងត្រូវបានប៉ាតង់) យើងបានញែកមេរោគ H5N1 ចំនួនប្រាំមួយប្រភេទចេញពីបសុបក្សី និងហ្គ្រេបបេ (Podiceps cris tatus) ជាមួយនឹងកំហាប់ជាលិកាខ្ពស់នៃមេរោគ។ ជាមួយនឹងអាទិភាពចុះថ្ងៃទី 8 ខែសីហា ឆ្នាំ 2005 ប្រភេទទាំងនេះត្រូវបានដាក់ក្នុងបណ្តុំរដ្ឋនៃមេរោគ ហើយទិន្នន័យលំដាប់លំដោយនៃហ្សែនពេញរបស់ពួកគេត្រូវបានដាក់ក្នុង GenBank ជាមួយនឹងអាទិភាពចុះថ្ងៃទី 5 ខែកញ្ញា ឆ្នាំ 2005 ។ ទីតាំងនៃការកាត់ proteolytic នៃ hemagglutinin នៃពូជដែលទទួលបានទាំងអស់មានផ្ទុកនូវលំដាប់អាស៊ីតអាមីណូ PQGERRRKKRGLF ដែលជាលក្ខណៈនៃមេរោគគ្រុនផ្តាសាយបក្សីដែលបង្កជំងឺយ៉ាងខ្លាំង។ លំដាប់នុយក្លេអូទីតនៃហ្សែន hemagglutinin នៃមេរោគបក្សីដែលបានវិភាគទាំងអស់បានប្រែទៅជាដូចគ្នាទាំងស្រុង ប៉ុន្តែខុសគ្នាពីប្រភេទដែលដាច់ឆ្ងាយពីបក្សីព្រៃ (ហ្គ្រេប) ទោះបីជាមានការជំនួសនុយក្លេអូទីតពីរក៏ដោយ (រូបភាពទី 3)។ ការវិភាគផ្នែករូបវិទ្យាបានបង្ហាញពីកម្រិតខ្ពស់នៃភាពដូចគ្នារវាង hemagglutinins នៃពូជស៊ីបេរីខាងលិច និងពូជដែលនៅដាច់ពីគេនៅនិទាឃរដូវនៃឆ្នាំដូចគ្នាពី goose ដែលមានក្បាលរបារ (Anser indicus) នៅលើបឹង។ Kukunar នៅភាគពាយព្យនៃខេត្ត Qinghai (PRC) ។ នេះត្រូវបានបញ្ជាក់យ៉ាងពេញលេញនៅពេលវិភាគហ្សែនចំនួនប្រាំពីរដែលនៅសល់។
អត្តសញ្ញាណនៃលក្ខណៈហ្សែននៃពូជដាច់ស្រយាលបង្ហាញពីទំនាក់ទំនងផ្ទាល់រវាងមេរោគដែលកំពុងចរាចរនៅក្នុងចំនួនប្រជាជននៃសត្វស្លាបព្រៃ និងក្នុងស្រុក។ ក្នុងពេលជាមួយគ្នានេះ មេរោគផ្តាសាយបក្សីប្រភេទ H5N1 ដែលបានរកឃើញក្នុងឆ្នាំ 2005 មានភាពខុសប្លែកគ្នាយ៉ាងខ្លាំងពីប្រភេទវីរុសនេះ ដែលដាក់ឱ្យនៅដាច់ពីគេកាលពីឆ្នាំមុន រួមទាំងប្រភេទ A/Vietnam/1194/2004(H5N1) ដែលទទួលបានពីប្រទេសអង់គ្លេស ដែលត្រូវបានផ្តល់ជូននៅក្នុងប្រទេសរបស់យើងសម្រាប់ ការផលិតវ៉ាក់សាំង។ វាច្បាស់ណាស់ថា យ៉ាងហោចណាស់សម្រាប់វ៉ាក់សាំងពេទ្យសត្វ មានតែប្រភេទមេរោគពីការប្រមូលរដ្ឋនៃមេរោគដែលត្រូវនឹងលក្ខណៈសម្បត្តិអង់ទីហ្សែននៃមេរោគដែលកំពុងចរាចរនៅក្នុងប្រទេសរុស្ស៊ីប៉ុណ្ណោះដែលអាចប្រើបាន។
ពូជដែលយើងដាក់ឱ្យនៅដាច់ពីគេ ដែលដាក់ក្នុងបណ្តុំនៃមេរោគរបស់រដ្ឋ ត្រូវបានគេប្រើប្រាស់រួចហើយសម្រាប់ការផលិតវ៉ាក់សាំងទ្រង់ទ្រាយធំនៅកសិដ្ឋានចិញ្ចឹមបសុបក្សី Stavropol របស់សហព័ន្ធរដ្ឋសហព័ន្ធ។ បសុបក្សីកំពុងត្រូវបានគេចាក់វ៉ាក់សាំងនៅស្រុកសហព័ន្ធភាគខាងត្បូង។ ត្រឹមថ្ងៃទី 15 ខែមិថុនា ឆ្នាំ 2006 វាត្រូវបានគេគ្រោងនឹងផលិតវ៉ាក់សាំងចំនួន 15 លានដូស ជាមួយនឹងការពង្រីកផលិតកម្មបន្ថែមទៀត។
ដោយវិធីនេះ នៅក្នុងជំងឺរាតត្បាត នៅពេលដែលវាចាំបាច់ដើម្បីបង្កើតការផលិតវ៉ាក់សាំងយ៉ាងឆាប់រហ័ស វាត្រូវបានណែនាំឱ្យប្រើខ្សែកោសិកាដែលមេរោគគ្រុនផ្តាសាយប្រមូលផ្តុំយ៉ាងលឿនក្នុងកំហាប់ខ្ពស់ជាស្រទាប់ខាងក្រោម។ វិធីសាស្ត្រដែលទើបបង្កើតថ្មីនេះមានគុណសម្បត្តិយ៉ាងសំខាន់ជាងវិធីបុរាណដែលប្រើ

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
អំប្រ៊ីយ៉ុងមាន់ត្រូវបានបង្កើតឡើង៖ ខណៈពេលដែលដែន antigenic ទាំងអស់នៃ hemagglutinin ត្រូវបានបម្រុងទុក វ៉ាក់សាំងវប្បធម៌នឹងលុបបំបាត់ការកើតឡើងនៃផលវិបាកដែលទាក់ទងនឹងប្រូតេអ៊ីនមាន់។ នេះមានសារៈសំខាន់ជាពិសេសនៅពេលផលិតវ៉ាក់សាំងសម្រាប់មនុស្ស។ អ្នកគ្រាន់តែត្រូវដឹងថាតើសំពាធប្រភេទណាដែលគួរប្រើ ដើម្បីការពារមនុស្ស។ នេះនឹងអាស្រ័យលើទម្រង់អង់ទីហ្សែននៃវ៉ារ្យ៉ង់រាតត្បាតដែលកំពុងកើតមាន។ ប្រហែលជាវានឹងខុសពីអ្វីដែលវាឥឡូវនេះ។ ក្នុងករណីណាក៏ដោយ ការប្រើប្រាស់វ៉ាក់សាំងបន្តផ្ទាល់ គឺពិតជាមិនអាចទទួលយកបានឡើយ។ អន្តរកម្មហ្សែនរវាងវ៉ាក់សាំង និងមេរោគក្នុងវាលអាចនាំទៅដល់ការលេចចេញនូវអ្នកធានាឡើងវិញជាមួយនឹងផលវិបាកដែលមិនអាចទាយទុកជាមុនបាន។
រូប ៣. កម្រិតនៃភាពពាក់ព័ន្ធនៃលំដាប់នុយក្លេអូទីតនៃហ្សែន hemagglutinin នៃមេរោគគ្រុនផ្តាសាយ A ប្រភេទរង H5 វ៉ារ្យ៉ង់ដាច់ដោយឡែកពីសត្វស្លាបព្រៃ និងក្នុងស្រុកនៅក្នុងប្រទេសផ្សេងៗគ្នាក្នុងរយៈពេល 10 ឆ្នាំកន្លងមកនេះ។ ប្រភេទមេរោគ H5N1 ដ៏ខ្ពស់នៃក្រុមវីរុស Qinghai-Novosibirsk ត្រូវបានគូសបញ្ជាក់ជាដិត។
ការវិភាគហ្សែននៃពូជដែលយើងញែកដាច់ពីគេបានបង្ហាញពីលក្ខណៈពិសេសមួយចំនួនដែលទាក់ទងនឹងលក្ខណៈសម្បត្តិជីវសាស្រ្ត។ បន្ថែមពីលើលំដាប់អាស៊ីតអាមីណូនៃកន្លែងបំបែក proteolytic នៃ hemagglutinin ដែលកំណត់កម្រិតខ្ពស់នៃការបង្កជំងឺនៃមេរោគ ការលុបត្រូវបានរកឃើញនៅទីតាំង 49-68 ក្នុង neuraminidase (genotype Z) ដែលបង្ហាញពីការកើនឡើងនៃមេរោគដែលយើងមាន។ ដាច់ដោយឡែកសម្រាប់បសុបក្សី និងសក្តានុពលបង្កជំងឺសម្រាប់មនុស្ស។ អាស៊ីត glutamic នៅទីតាំង 92 នៃប្រូតេអ៊ីន NS1 កំណត់ភាពធន់នៃមេរោគទៅនឹង interferon និងការកើនឡើងនៃមេរោគនៅក្នុងជ្រូក។ លីស៊ីននៅទីតាំង 627 នៃប្រូតេអ៊ីន PB2 ពន្យល់ពីសមត្ថភាពនៃប្រភេទដែលបានសិក្សាក្នុងការបន្តពូជនៅក្នុងកោសិកាថនិកសត្វផ្សេងៗ។ លក្ខណៈសម្បត្តិដែលបានកំណត់អត្តសញ្ញាណនៃមេរោគដែលបានចូលទៅក្នុងប្រទេសរុស្ស៊ីបង្ហាញពីការបង្ករោគខ្ពស់របស់វាចំពោះបក្សី និងមនុស្ស។
វត្តមានរបស់ serine និងមិនមែន asparagine នៅក្នុងទីតាំងទី 31 នៃ M2 បង្ហាញពីភាពប្រែប្រួលនៃមេរោគចំពោះ rimantadine ដែលស្របគ្នាទាំងស្រុងជាមួយនឹងទិន្នន័យពីការសិក្សាដោយផ្ទាល់អំពីឥទ្ធិពលនៃថ្នាំប្រឆាំងមេរោគលើការបន្តពូជរបស់មេរោគ។ សម្រាប់គោលបំណងទាំងនេះ យើងក៏បានប្រើខ្សែកោសិកា ហើយបានរកឃើញថា សម្រាប់ការបង្ការ និងការព្យាបាលដំបូងនៃជំងឺគ្រុនផ្តាសាយ ទាំងថ្នាំបរទេសដែលមានតម្លៃថ្លៃ - ឧទាហរណ៍ ថ្នាំ Tamiflu និងថ្នាំក្នុងស្រុកដែលមានតម្លៃថោកដែលមាននៅក្នុងឱសថស្ថាន - remantadine មានប្រសិទ្ធភាពស្មើគ្នា និងអាច ត្រូវបានប្រើ។

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
virazole (សម្រាប់ការប្រើប្រាស់តាមសរសៃឈាម និង aerosol), arbidol ។ ជាអកុសល ការផលិតថ្នាំទាំងនេះបច្ចុប្បន្នអវត្តមាន ឬមិនគ្រប់គ្រាន់នៅក្នុងប្រទេស ហើយវាជារឿងបន្ទាន់ក្នុងការបង្កើតទុនបម្រុងយុទ្ធសាស្ត្ររបស់ពួកគេ។
តើមេរោគគ្រុនផ្តាសាយ H5N1 ឆ្លងចូលរុស្សីដោយរបៀបណា និងនៅពេលណា ហើយតើព្រឹត្តិការណ៍បន្តទៀតនឹងវិវឌ្ឍន៍យ៉ាងដូចម្តេច?
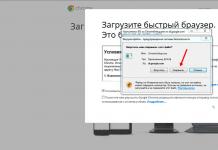
រូប ៤. ផ្លូវនៃការរីករាលដាលនៃមេរោគផ្ដាសាយ H5N1 នៅក្នុងសត្វបក្សីព្រៃ និងក្នុងស្រុក។ មេរោគគ្រុនផ្តាសាយទាបបង្កជំងឺ (LPIVs) ដាច់ដោយឡែកពីសត្វស្លាបព្រៃ និងក្នុងស្រុកនៅតំបន់ភាគខាងជើងភាគខាងកើតនៃដែនដី Altai ក្នុងឆ្នាំ 1991 និងនៅភាគខាងត្បូងនៃដែនដី Primorsky ក្នុងឆ្នាំ 2001 ជាក់ស្តែងគឺជាបុព្វហេតុនៃការផ្ទុះឡើងនៃជំងឺផ្តាសាយនៅក្នុងទីក្រុងហុងកុងក្នុងឆ្នាំ 1997 និង epizootics នៅអាស៊ីអាគ្នេយ៍ក្នុងឆ្នាំ 2003-2005 ក៏ដូចជានៅភាគពាយព្យនៃប្រទេសចិនក្នុងឆ្នាំ 2005 ។ ដោយបានក្លាយទៅជាភ្នាក់ងារបង្ករោគខ្ពស់ (HPPV) មេរោគទាំងនេះបានជ្រាបចូលក្នុងអំឡុងពេលនៃការធ្វើចំណាកស្រុកនៃបក្សីព្រៃនៅនិទាឃរដូវទៅកាន់តំបន់ស៊ីបេរីខាងលិច ដែលពួកគេបណ្តាលឱ្យមានការផ្ទុះឡើងនៃជំងឺគ្រុនផ្តាសាយនៅរដូវក្តៅ។ ឆ្នាំ 2005 ក្នុងចំណោមបសុបក្សី។ ក្នុងអំឡុងពេលនៃការធ្វើចំណាកស្រុកនៃសត្វស្លាបក្នុងទឹក និងពាក់កណ្តាលទឹក វីរុស HPV បានរីករាលដាលបន្ថែមទៀតទៅភាគខាងជើង និងខាងលិចនៃអឺរ៉ាស៊ី ហើយក្នុងរដូវរងាឆ្នាំ ២០០៦ មេរោគទាំងនេះត្រូវបានរកឃើញរួចហើយនៅក្នុងទ្វីបអាហ្រ្វិក។ ព្រួញក្រាស់បង្ហាញពីការឆ្លងមេរោគគ្រុនផ្តាសាយពីព្រៃ
បក្សីទៅផ្ទះ និងផ្ទុយមកវិញ។
ទីមួយ ប្រភេទមេរោគទាបដែលចរាចរនៅស៊ីបេរី និងចុងបូព៌ាក្នុងចំណោមសត្វស្លាបព្រៃត្រូវបានណែនាំក្នុងអំឡុងពេលធ្វើចំណាកស្រុករដូវស្លឹកឈើជ្រុះទៅកាន់បណ្តាប្រទេសអាស៊ីអាគ្នេយ៍ (រូបភាពទី 4) ។ ដោយបានក្លាយជាអ្នកបង្កជំងឺខ្លាំងនៅទីនោះ ពួកគេរួមជាមួយនឹងសត្វស្លាបព្រៃបានចូលតំបន់ស៊ីបេរីខាងលិចនៅនិទាឃរដូវឆ្នាំ 2005 ហើយកាន់តែសកម្មក្នុងអំឡុងពេលដែលកូនមាន់បានបង្ហាញខ្លួន។ មេរោគបង្កជំងឺខ្លាំងបានសាយភាយជាមួយសត្វស្លាបទៅកន្លែងសំបុកលើផ្ទៃដីជាង ១០ លានក្បាល។
គីឡូម៉ែត្រ ២ ។ បន្ទាប់ពីមេរោគបានចូលទៅក្នុងហ្វូងសត្វបក្សី ការផ្ទុះឡើងនៃមេរោគអេពីសហ្សូទីកបានកើតឡើង។ នេះគឺធ្ងន់ធ្ងរនិងយូរអង្វែង។
ការព្យាករណ៍ទីបីគឺថានៅពេលដែលសត្វស្លាបហើរត្រឡប់ទៅកន្លែងរដូវរងារបស់ពួកគេនៅរដូវស្លឹកឈើជ្រុះតាមរយៈតំបន់ដែលមានប្រជាជនច្រើននៃប្រទេសរុស្ស៊ីនិងប្រទេសដទៃទៀតពួកគេនឹងរីករាលដាលមេរោគម្តងទៀត។

B OLOGY និងវិទ្យាសាស្ត្រវេជ្ជសាស្ត្រ | មេរោគគ្រុនផ្តាសាយ៖ ព្រឹត្តិការណ៍ និងការព្យាករណ៍ |
ហើយដូច្នេះវាបានកើតឡើង។ នៅរដូវស្លឹកឈើជ្រុះឆ្នាំ 2005 មេរោគនេះបានទៅដល់ប្រទេសអឺរ៉ុបភាគច្រើនរួចហើយ វាក៏ត្រូវបានគេរកឃើញនៅក្នុងប្រទេសទួរគី គ្រីមៀ អ៊ីរ៉ង់ អាស៊ែបៃហ្សង់ ហ្សកហ្ស៊ី ឥណ្ឌា និងនៅអាហ្វ្រិកផងដែរ។ ហើយនៅទីនេះយើងបានទៅដល់ Tula, Kalmykia និងតំបន់ដីសណ្ត Volga ដែលជាកន្លែងដែលការផ្ទុះឡើងនៃជំងឺគ្រុនផ្តាសាយនៅក្នុងប្រជាជន Swan ស្លូត (Cygnusolor) បានកើតឡើងនៅក្នុងខែធ្នូឆ្នាំ 2005 បន្ទាប់ពីការឈប់សម្រាកខ្លីនៃសត្វទាភាគខាងជើង - ទា tufted (Aythya fuligula) ។ ពូជដែលដាច់ឆ្ងាយពីសត្វស្វា យោងតាមការវិភាគហ្សែនម៉ូលេគុលរបស់វាក៏ជាកម្មសិទ្ធិរបស់ក្រុមវីរុស Qinghai-West Siberian ផងដែរ។ ក្នុងរយៈពេលជាងប្រាំមួយខែនៃការចរាចរក្នុងចំណោមសត្វស្លាបព្រៃ ពូជនេះរក្សាបាននូវប្រភេទសត្វរបស់វា ហើយមិនបាត់បង់ការបង្ករោគខ្ពស់របស់វាឡើយ។
ការព្យាករណ៍ទីបួនគឺជាការប្រកាសអាសន្នបំផុត។ មេរោគនេះបានបំពុលសាកសពទឹកជាច្រើននៅក្នុងតំបន់សំបុក និងនៅលើផ្លូវហោះហើរ ហើយវានឹងបន្តនៅទីនោះរហូតដល់រដូវផ្ការីក។ រាល់រាងកាយធម្មជាតិនៃទឹកដែលមានលាមកពីសត្វស្លាបដែលមានមេរោគប្រែទៅជា "គ្រាប់បែកពេលវេលា" ។ នេះអាចប្រៀបធៀបទៅនឹងការចូលរួមរបស់ peatlands នៅក្នុងភ្លើង taiga ។ នៅនិទាឃរដូវ សត្វស្លាបដែលឆ្លងមេរោគ និងមានសុខភាពល្អនឹងត្រលប់មកវិញ ហើយហោះហើរឆ្លងកាត់ "វាលមីន" ទាំងនេះ ដូច្នេះព្រឹត្តិការណ៍នៅក្នុងរដូវក្តៅឆ្នាំ 2006 អាចមានគ្រោះថ្នាក់ជាងរដូវកាលមុន។ នេះត្រូវបានបញ្ជាក់ដោយការធ្លាក់ចុះខ្លាំងដូចជាការធ្លាក់ព្រិលនៃស្ថានការណ៍នៅអឺរ៉ុប អាស៊ី និងអាហ្រ្វិករួចហើយកាលពីខែមីនា។ នេះគឺជា panzootic រួចទៅហើយ។ ហើយនៅពេលដែលប្រភេទសត្វដែលបង្កជំងឺខ្លាំងដែលកំពុងចរាចរក្នុងចំណោមសត្វស្លាបព្រៃនៅរដូវផ្ការីក ត្រលប់មករកមេរោគទាបវិញ វាមិនអាចទៅរួចទេក្នុងការទស្សន៍ទាយថាតើដំណើរការនៃការចាត់ថ្នាក់របស់ពួកគេនឹងត្រូវចំណាយពេលប៉ុន្មានខែ ឬច្រើនឆ្នាំ។ វាច្បាស់ណាស់ថានេះគឺជាប្រធានបទនៃការសិក្សាជាអាទិភាព ដែលការវិវត្តនៃព្រឹត្តិការណ៍នាពេលខាងមុខអាស្រ័យ។
ចំណែកជំងឺរាតត្បាតវិញ ក៏អាចកើតមានក្នុងប្រទេសយើងដែរ បន្ទាប់ពីជ្រូកឆ្លងមេរោគមនុស្ស និងសត្វបក្សី។ ប៉ុន្តែវាទំនងជានឹងមករកយើងពីប្រទេសចិន ដែលលទ្ធភាពនៃការផ្លាស់ប្តូរអ្នកផ្តល់ជំនួយគឺអស្ចារ្យជាពិសេស ដោយសារសកម្មភាពនៃដំណើរការអេពីហ្សូទិក និងកត្តាងាយរងគ្រោះដ៏ធំក្នុងចំណោមប្រជាជន។ មេរោគរាតត្បាតអាចលេចឡើងក្នុងប្រទេសរបស់យើងគ្រប់ពេលវេលា - សម្រាប់បញ្ហានេះ ការជំនួសអាស៊ីតអាមីណូមួយនៅក្នុង PCC នៃ hemagglutinin គឺគ្រប់គ្រាន់ហើយ ជាលទ្ធផលមេរោគនឹងចាប់ផ្តើមទទួលស្គាល់អ្នកទទួលនៃកោសិកាមនុស្ស ហើយតាមនោះនឹងចាប់ផ្តើម។ ឆ្លងពីមនុស្សទៅមនុស្ស។
អ្វីដែលតាមទស្សនៈរបស់យើងគួរធ្វើឥឡូវនេះនៅកម្រិតរដ្ឋត្រូវបានបង្កើតឡើងក្នុងតារាង។ យើងនឹងយកចិត្តទុកដាក់ជាពិសេសក្នុងការសិក្សាអំពីការវិវត្តន៍បន្ថែមទៀតនៃប្រភេទបង្កជំងឺខ្ពស់ ដែលបានប៉ះពាល់ដល់ចំនួនសត្វស្លាបព្រៃ។ ប្រព័ន្ធអេកូឡូស៊ីនៅលើទឹកដីរុស្ស៊ីមានសារៈសំខាន់សំខាន់ក្នុងរឿងនេះ។ យើងគ្រោងនឹងបន្តការឃ្លាំមើលនៅក្នុងផ្នែកអ៊ឺរ៉ុបនៃប្រទេសនេះ នៅស៊ីបេរី និងចុងបូព៌ា ហើយក៏អាចនៅក្នុងប្រទេសជិតខាងមួយចំនួនផងដែរ។
ក្នុងរយៈពេលប្រាំឆ្នាំកន្លងមកនេះ ការស្រាវជ្រាវរបស់យើងត្រូវបានអនុវត្តរួមគ្នាជាមួយ gamewardens, ornithologists, និងបុគ្គលិកនៃ phyto-veterinary and sanitary services សហព័ន្ធនៃតំបន់ Novosibirsk, Astrakhan, Irkutsk, Primorsky Territory, Birobidzhan, the Republic of Kalmykia and ប៊ូរីតាយ៉ា។ ទាំងអស់នេះបានកើតឡើងនៅក្នុងក្របខ័ណ្ឌនៃកម្មវិធីសហព័ន្ធ "ការការពារប្រឆាំងនឹងភ្នាក់ងារបង្ករោគ", "ការអភិវឌ្ឍមធ្យោបាយនិងវិធីសាស្រ្តសម្រាប់ការប្រឆាំងភេរវកម្មជីវសាស្រ្ត", "គ្រុនផ្តាសាយ A នៃជ្រូកនិងបក្សី: អន្តរកម្មនៃចំនួនប្រជាជន" ។
ពួកវាជាប៉ារ៉ាស៊ីតដែលជាប់កាតព្វកិច្ចក្នុងកោសិកា មានន័យថាពួកគេមិនអាចចម្លង ឬឆ្លងកាត់ហ្សែនរបស់ពួកគេដោយគ្មានជំនួយឡើយ។ ភាគល្អិតមេរោគតែមួយ (virion) គឺខ្លួនវាអសកម្ម។ នៅពេលដែលមេរោគឆ្លងទៅកោសិកាមួយ វាប្រើអង់ស៊ីម និងរចនាសម្ព័ន្ធកោសិកាភាគច្រើនដើម្បីចម្លង។
មិនដូចអ្វីដែលយើងឃើញនៅក្នុងដំណើរការបែងចែកកោសិកាដូចជា និង ការចម្លងមេរោគបង្កើតកូនចៅជាច្រើនដែលបំផ្លាញកោសិកាមេ ហើយបន្ទាប់មកឆ្លងកោសិកាផ្សេងទៀតនៅក្នុងខ្លួន។
សម្ភារៈហ្សែនមេរោគ
មេរោគអាចមាន DNA ឬ RNA ខ្សែតែមួយ/ពីរខ្សែ។ ប្រភេទនៃសម្ភារៈហ្សែនដែលរកឃើញនៅក្នុងមេរោគជាក់លាក់មួយអាស្រ័យលើធម្មជាតិ និងមុខងាររបស់វា។ លក្ខណៈពិតប្រាកដនៃអ្វីដែលកើតឡើងបន្ទាប់ពីម៉ាស៊ីនត្រូវបានឆ្លងគឺប្រែប្រួលអាស្រ័យលើធម្មជាតិនៃមេរោគ។
ដំណើរការចម្លងនឹងខុសគ្នាសម្រាប់ dsDNA, ssDNA, dsRNA និងមេរោគ RNA តែមួយខ្សែ។ ជាឧទាហរណ៍ មេរោគ DNA ដែលមានខ្សែពីរដង ជាធម្មតាត្រូវតែចូលទៅក្នុងកោសិកាម៉ាស៊ីន មុនពេលពួកវាអាចចម្លងបាន។ ទោះជាយ៉ាងណាក៏ដោយ មេរោគ RNA តែមួយខ្សែចម្លងជាចម្បងទៅក្នុងកោសិកាម៉ាស៊ីន។
នៅពេលដែលមេរោគឆ្លងទៅម៉ាស៊ីន សមាសធាតុនៃមេរោគត្រូវបានផលិតដោយម៉ាស៊ីនកោសិកា ហើយការប្រមូលផ្តុំនៃមេរោគ capsid គឺជាដំណើរការដែលមិនមែនជាអង់ស៊ីម។ ជាធម្មតាមេរោគអាចឆ្លងបានតែចំនួនម៉ាស៊ីនដែលមានកំណត់ប៉ុណ្ណោះ។ យន្តការ "ចាក់សោនិងសោ" គឺជាការពន្យល់ទូទៅបំផុតសម្រាប់បាតុភូតនេះ។ ប្រូតេអ៊ីនជាក់លាក់នៅលើភាគល្អិតមេរោគត្រូវតែផ្គូផ្គងប្រូតេអ៊ីនទទួលជាក់លាក់នៅលើផ្ទៃក្រឡានៃម៉ាស៊ីនជាក់លាក់មួយ។
តើមេរោគឆ្លងកោសិកាដោយរបៀបណា?
ដំណើរការជាមូលដ្ឋាននៃការឆ្លងមេរោគ និងការចម្លងមេរោគកើតឡើងក្នុង 6 ដំណាក់កាល៖
- ការស្រូបយក - មេរោគភ្ជាប់ទៅនឹងកោសិកាម៉ាស៊ីន។
- ធាតុចូល - មេរោគណែនាំហ្សែនរបស់វាទៅក្នុងកោសិកាម៉ាស៊ីន។
- ការចម្លងហ្សែនមេរោគ - ហ្សែនមេរោគត្រូវបានចម្លងដោយប្រើរចនាសម្ព័ន្ធកោសិការបស់ម៉ាស៊ីន។
- ការជួបប្រជុំគ្នា - សមាសធាតុមេរោគ និងអង់ស៊ីមត្រូវបានបង្កើតឡើង ហើយចាប់ផ្តើមប្រមូលផ្តុំ។
- ភាពចាស់ទុំ - មេរោគវិវត្តចេញពីសមាសធាតុដែលបានជួបប្រជុំគ្នា។
- ចេញ - មេរោគថ្មីបំបែកចេញពីកោសិកាម៉ាស៊ីនដើម្បីស្វែងរកជនរងគ្រោះថ្មីដើម្បីឆ្លង។
មេរោគអាចឆ្លងទៅគ្រប់ប្រភេទនៃកោសិកា រួមទាំង
ក្រុមគ្រួសារនៃមេរោគ orthomyxoviruses (ភាសាក្រិច orthos - ត្រឹមត្រូវ tukha - mucus) រួមមានមេរោគគ្រុនផ្តាសាយប្រភេទ A, B, C ដែលដូចជា paramyxoviruses មានទំនាក់ទំនងនឹង mucin ។ មេរោគគ្រុនផ្តាសាយ A ឆ្លងដល់មនុស្ស និងប្រភេទសត្វមួយចំនួន (សេះ ជ្រូក។ល។) និងបក្សី។ មេរោគគ្រុនផ្តាសាយប្រភេទ B និង C គឺជាភ្នាក់ងារបង្ករោគសម្រាប់តែមនុស្សប៉ុណ្ណោះ។ មេរោគគ្រុនផ្តាសាយមនុស្សដំបូងគេត្រូវបានញែកដាច់ពីមនុស្សក្នុងឆ្នាំ 1933 ដោយ W. Smith, C. Andrews និង P. Ladow (ប្រភេទ WS) ដោយឆ្លងមេរោគពណ៌ស។ ក្រោយមក មេរោគនេះត្រូវបានចាត់ថ្នាក់ជាប្រភេទ A. នៅឆ្នាំ 1940 T. Francis និង T. Megill បានរកឃើញមេរោគគ្រុនផ្តាសាយប្រភេទ B ហើយនៅឆ្នាំ 1949 R. Taylor បានរកឃើញមេរោគគ្រុនផ្តាសាយប្រភេទ C។ នៅពេលដែលចាត់ថ្នាក់មេរោគគ្រុនផ្តាសាយ តែងតែមាន ការលំបាកមួយចំនួនដែលទាក់ទងនឹងភាពប្រែប្រួលនៃអង់ទីហ្សែនរបស់ពួកគេ។ មេរោគគ្រុនផ្តាសាយត្រូវបានបែងចែកជាបីប្រភេទ A, B និង C. ប្រភេទ A រួមមានប្រភេទរងជាច្រើនដែលខុសគ្នាពីគ្នាទៅវិញទៅមកនៅក្នុងអង់ទីកររបស់ពួកគេ - hemagglutinin និង neuraminidase ។ យោងតាមការចាត់ថ្នាក់របស់អង្គការសុខភាពពិភពលោក (1980) មេរោគគ្រុនផ្តាសាយមនុស្ស និងសត្វប្រភេទ A ត្រូវបានបែងចែកជា 13 ប្រភេទរងអង់ទីហ្សែនសម្រាប់ hemagglutinin (H1-H13) និង 10 សម្រាប់ neuraminidase (N1-N10) ។ ក្នុងចំណោមនោះ មេរោគគ្រុនផ្តាសាយមនុស្សប្រភេទ A រួមមាន hemagglutinins បី (HI, H2 និង H3) និង neuraminidases ពីរ (N1 និង N2) សម្រាប់វីរុសប្រភេទ A ប្រភេទរងនៃ hemagglutinin និង neuraminidase ត្រូវបានចង្អុលបង្ហាញនៅក្នុងវង់ក្រចក។ ឧទាហរណ៍ មេរោគគ្រុនផ្តាសាយ A៖ Khabarovsk/90/77 (H1N1)។